[이데일리 김새미 기자]
올릭스(226950)는 비대흉터치료제 ‘OLX101A’ 미국 임상 2a상 톱라인(topline) 결과 인체 내에서 임상 효력을 확인했다고 27일 밝혔다.
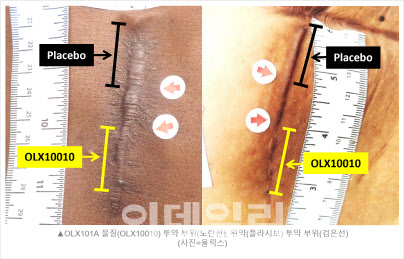 | | 올릭스의 비대흉터치료제 ‘OLX101A’와 위약을 투여한 모습 (사진=올릭스) |
|
이날 올릭스는 OLX101A 미국 임상 2a상에 대한 톱라인 결과를 수령했다. 해당 임상은 2020년 10월 미국 식품의약국(FDA)의 승인을 받아 미국 내 5개 시험기관에서 실시됐다. OLX101A 저용량과 위약군, OLX101A 고용량과 위약군으로 10명씩 2그룹으로 나눠 총 20명을 대상으로 임상을 진행했다.
OLX101A의 1차 평가지표는 흉터 재건술로부터 24주 시점에 연구자의 흉터평가척도(POSAS) 스코어를 이용해 비대흉터의 재발 정도를 비교하는 것이다. 1차 평가지표는 1부터 10까지의 숫자로 측정된 베이스라인(Baseline, 투약 전) 흉터의 심각도를 투약 24주 후 재측정해 흉터의 개선 정도를 수치로 측정하도록 설계됐다. 심각도 점수가 낮을수록 정상 피부에 가깝다는 의미다.
이번 톱라인 결과에 따르면 시험군의 1차 평가지표 p값(p-value)은 0.017로 통계적 유의성을 충족했다. 반면 위약을 투여한 대조군의 p값은 0.065로 통계적 유의성이 확인되지 않았다. 시험군 베이스라인의 평균 POSAS 스코어는 5.1점이었으며, 투약 24주 후 POSAS 스코어는 3.3점으로 평균 1.8점이 감소했다. 대조군 베이스라인의 평균 POSAS 스코어는 5점이었으며, 투약 24주 후 POSAS 스코어는 3.8점으로 평균 1.2점 줄었다. 투약 24주 후 시험군과 대조군간 비교 결과는 공개하지 않았다.
올릭스는 추후 안전성 평가 등 2차 평가지표가 포함된 임상결과보고서(CSR)를 수령할 예정이다. 올릭스는 이번 임상 결과를 바탕으로 해당 치료제에 관심을 보이는 글로벌 제약사와 파트너링을 추진할 계획이다.
이동기 올릭스 대표이사는 “비대흉터 치료제의 2상 임상시험 톱라인 결과에서 통계적으로 유의미한 임상 효력이 확인된 것은 올릭스에서 개발 중인 치료제 중 최초로 휴먼 PoC(개념 증명)를 확보한 것으로 대단히 고무적인 성과“라고 강조했다.










![[포토] 원·달러 환율 오를까?](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900849t.jpg)
![[포토] 폭설 피해](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900576t.jpg)
![[포토] 주식시장 활성화 테스크포스-경제계 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900547t.jpg)
![[포토]최재해, '정치적 탄핵 매우 유감...자진 사퇴 생각 없다'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900431t.jpg)
![[포토]'모두발언하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900370t.jpg)
![[포토]이데일리 퓨처스포럼 송년회 무대](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801622t.jpg)
![[포토]용산국제업무지구 개발계획 공동협약식에서 협약서 서명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801123t.jpg)
![강 건너고 짐도 나르고…‘다재다능’ 이상이의 무한변신 차는[누구차]](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24113000161h.jpg)



