[이데일리 양지윤 기자]
엔케이맥스(182400)는 미국 자회사 엔케이젠바이오텍이 “동정적 사용 승인을 통해 치료를 진행한 육종암 말기 환자에게서 암이 완전히 사라진 것으로 나타났다”고 14일 밝혔다. 동정적 사용은 환자가 적절한 치료제가 없어 치료를 포기할 상황에 이를 경우 의료당국이 시판 승인 전 신약을 무상으로 공급, 치료 기회를 주는 제도를 일컫는다.
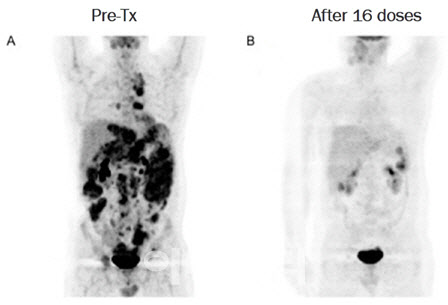 | | SNK01(슈퍼NK) 병용투여 전(A)과 후(B) 종양 소멸 비교 사진.(사진=엔케이맥스) |
|
엔케이맥스는 지난해 12월 해당 환자의 간에 발생한 종양이 약 80% 관해(암이 완전히 사라진 상태)됐다고 공개한 바 있다. 육종암의 일종인 결합조직성소원형세포종(DSRCT) 환자로 미국 식품의약국(FDA)로부터 동정적사용 승인을 받아 슈퍼NK와 머크의 키트루다를 병용, 치료를 진행했다.
이 환자는 2017년 육종암 판정을 받을 당시 간, 폐, 복부, 방광 등 전신에 암이 전이된 상태였다. 슈퍼NK 투약 전 약 1년 반 동안 화학치료제와 면역항암제를 투여했으나 독성 반응이 나타나고 암이 계속 커져 치료를 중단했다. 이 환자는 PD-L1 발현율이 음성인 환자였다.
이후 이 환자는 동정적 사용 환자로 등록돼 28개월동안 총 30회 슈퍼NK와 키트루다를 병용투여 받았다. PET-CT 검사 결과 잔존 종양이 존재하지 않는 것으로 관찰되어 완전관해 상태에 도달했다는 것이 회사측의 설명이다.
김혜련 연세암병원 종양내과 교수는 “말기 육종암은 치료가 매우 어렵고 예후가 좋지 않은 것이 현실”이라며 “육종암은 희귀성 난치암이기 때문에 효과적인 치료제가 아직 개발되지 않다. 수술요법, 방사선요법, 화학요법을 삼중병용해 사용하는 것이 유일한 표준치료 방법”이라고 말했다.
이어 김 교수는 “PD-L1 발현이 거의 없는 음성인 환자에게서 치료반응이 보인 것은 드문 사례로, 전체 암 환자 중 25~30% 만이 PD-L1 양성 환자이고 70~75%는 PD-L1 음성 환자로 알려져 있다”며 “만약 슈퍼NK가 PD-L1 음성 환자군을 양성 환자로 변화시킬 수 있다면 암 치료제 시장의 큰 변화를 이끌어낼 수 있을 것”이라고 덧붙였다.








![[포토]우리 이웃을 위한 크리스마스 선물](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122500173t.jpg)
![[포토]메리크리스마스](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400797t.jpg)
![[포토]즐거운 눈썰매](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400779t.jpg)
![[포토]취약계층 금융 부담 완화, '인사말하는 이재연 원장'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400633t.jpg)
![[포토]국민의힘 의원총회, '모두발언하는 권성동 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400506t.jpg)
![[포토]윤석열 대통령 탄핵심판 첫 변론 준비기일 27일 예정대로 진행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400433t.jpg)
![[포토]'더불어민주당 원내대책회의'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400387t.jpg)
![[포토]국무회의 입장하는 한덕수 권한대행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400378t.jpg)
![[포토]은행권 소상공인 금융지원 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300609t.jpg)
![[포토]인사청문회 출석한 마은혁 헌법재판관 후보자](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300404t.jpg)




