|
실제 비보존 제약(082800)은 지난달 7일 비마약성 진통제 ‘오피란제린’ 임상 3상 결과를 톱라인(결과 요약본)인지, 임상시험결과보고서(CSR)인지 명확히 알 수 없는 형태로 공시했다. 거래소 가이드라인에는 톱라인 데이터 또는 임상시험결과보고서(CSR)을 제출받았을 때만 공시해야 한다고 명시돼 있다. 하지만 회사가 제출한 공시 제목은 ‘유효성 일차평가항목 결과 발표’였고, 거래소는 이를 그대로 공시하도록 했다. 결국 비보존제약은 6일 정정공시를 통해 공시 제목을 ‘톱라인 결과 발표’로 수정했다.
가이드라인이 본격적으로 시행되면 투자자 혼란을 줄일 수 있는 통일성이 높아진 공시들을 기대할 수 있을 전망이다.
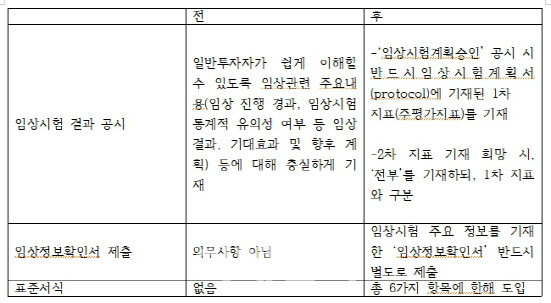
거래소는 이번 가이드라인에서 1차 지표 공시를 의무화했다. 임상시험계획승인 공시나 임상시험결과 공시에 임상시험계획서에 기재된 1차 지표(주평가지표)를 반드시 기재하라고 했다. 특히 1차 지표에 대한 하위 분석 또는 2차 지표가 중요 정보에 해당할 경우, 일부 유리한 정보만 선택적으로 제공하지 않도록 1차 지표의 하위지표, 2차 지표 전부를 기재하도록 했다.
실제 임상 결과를 발표하는 과정에서 2차 지표가 중요 데이터에 해당하는데도 데이터를 ‘선택적’으로만 공시한 사례도 있다.
근위축성 측삭경화증(ALS, 루게릭병) 치료제를 개발 중인 한 코스닥 바이오 기업은 임상2a상 톱라인 공시에서 유효성 데이터를 전혀 포함시키지 않았다. 통상 임상 2상은 안전성과 함께 유효성을 평가하는 것이 주목적이고, 회사도 2차 지표로 유효성을 측정할 10가지 평가지표를 설정해 놨다. 하지만 유효성 결과는 공시에 전혀 언급하지 않았다. 당시 주주들 사이에서는 공시가 혼란스럽다는 반응이 나왔다.
정윤택 제약산업전략연구원장은 “공시가 뻥튀기 이슈가 있긴 하지만, 일반 투자자들 이해를 돕기 위해선 어느 정도의 데이터 기반으로 평가 의견을 제시하는 게 적절하지 않을까 생각한다”며 “임상 결과에 대한 부분은 업체와 임상시험수탁기관(CRO)이 가장 잘 알기 때문에 탄력적으로 적용해서 지표에 대한 해석도 허용해줘야 투자자 이해를 돕는 데 좋지 않을까 생각한다”고 말했다.
한 바이오 기업 대표는 “최종 판단은 식약처가 하겠지만 투자자들에게 임상 결과에 대해 회사의 평가 내용 등 상세한 의견을 주는 것에 대해서는 공감한다”며 “공시에서 별도 칸을 마련해서 회사의 자체 평가나 시사점 등 주관적인 내용을 넣는다든지, 투자자들이 충분히 구분할 수 있도록, 회사 입장에서 소명할 기회를 주는 것이라고 본다. 그게 투자자 판단을 돕는 것이라 생각한다”고 말했다.








![[포토] '금융권 공감의 장' 인사말하는 이병래 회장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600936t.jpg)
![[포토]경북 국립의대 신설 촉구, '참석자들에게 인사하는 한동훈'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600846t.jpg)
![[포토]손태승 전 회장, 영장실질심사 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600794t.jpg)
![[포토]정윤하 등장](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600056t.jpg)
![[포토]내년에 또보자 가을](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600715t.jpg)
![[포토]민주당 민생연석회의 참석하는 이재명 대표](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600655t.jpg)
![[포토] '소상공인 힘보탬 프로젝트' 발표](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600583t.jpg)
![[포토]정부, 국무회의에서 세번째 `김여사 특검법` 거부권 건의 의결](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600579t.jpg)
![[포토] 이즈나 데뷔](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112500181t.jpg)
![[포토]첫 싱글 '라스트 벨'로 돌아온 TWS](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112500118t.jpg)




![“270만원 화웨이 신상폰 살 수 있어요?” 中매장 가보니[르포]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24112601335h.jpg)