|
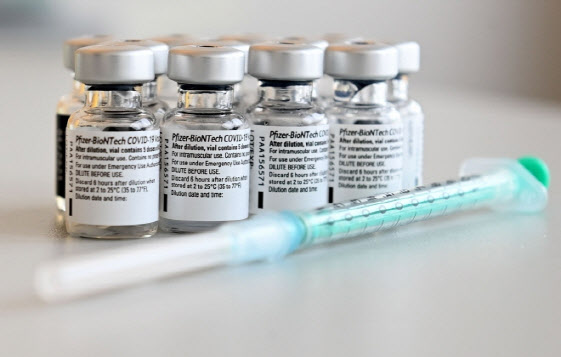
식품의약품안전처는 25일 한국화이자제약이 화이자 본사가 독일 바이오엔텍과 공동으로 개발한 코로나19 백신인 ‘코미나티주’의 품목허가를 신청해 허가심사에 착수했다고 밝혔다.
코로나19 바이러스의 항원 유전자를 mRNA 형태로 주입해 체내에서 항원 단백질을 생성함으로써 면역반응을 유도하는 방식으로, 제조 기간이 짧아 단기간에 대량 생산할 수 있다는 장점은 있지만 백신 보관 및 유통 시 초저온 냉동설비가 마련된 콜드체인 시스템이 필요하다.
화이자 코로나19 백신의 예상 접종 대상자는 만 16세 이상이다. 1회 접종 후 3주 후에 추가 접종하면 된다. 보관 조건은 회사에서 영하 60∼90℃에서 6개월로 신청했다.
이 가운데 EU에서는 약 4만 명에 대한 임상시험 결과 95%의 예방효과를 확인해 지난해 21일자로 조건부 허가됐다.






![[포토] 조사 마친 윤석열 대통령](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011501678t.jpg)
![[포토] 코스피, 코스닥 내림세...](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011501243t.jpg)
![[포토]'내란 우두머리 피의자' 윤석열 대통령 공수처로 이동](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011501058t.jpg)
![[포토] 네스프레소 2025 캠페인 론칭 토크쇼](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011501014t.jpg)
![[포토] '와일드무어' 미디어 행사](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011501005t.jpg)
![[포토]공수처 차고로 들어가는 윤 대통령 차량](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011500861t.jpg)
![[포토]사다리로 차벽 넘는 공수처](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011500701t.jpg)
![[포토]공개된 팰리세이드 풀체인지](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011500422t.jpg)
![[포토]공공기관 채용정보박람회 개최…“신규채용 2만4000명 추진”](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011400899t.jpg)
![[포토] 설 명절 자금 방출](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011400672t.jpg)
![[포토]박현경,백여 명의 팬들과 즐거운 출정식 개최](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25011200149h.jpg)



![뉴욕증시, 예상 밑돈 CPI·대형 은행주 호실적에 환호[월스트리트in]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25011600108h.jpg)