|
10일 제약 바이오업계에 따르면, 오는 20일은 이 회사가 식약처에 임상시험계획서를 제출한 지 영업일 기준 20일째 되는 날이다. 앞서 녹십자는 지난달 29일 식약처에 코로나19 혈장 치료제 임상 2상 시험계획서를 제출했다.
식약처는 지난 3월 코로나19 치료제·백신 개발을 위한 임상시험계획은 신속 심사에 나서 15일 이내 승인한다는 방침을 세웠다. 실제 식약처에 따르면 셀트리온(068270)의 항체 치료제 개발을 위한 임상 1상 시험계획은 계획서 접수 후 1주일 만에 승인됐다.
이에 따라 자료보완 등의 특이 사항이 없다면 GC녹십자의 임상 2상 시험계획은 이번주 승인될 것으로 예상된다. GC녹십자는 허가당국과 협의를 거쳐 임상 1상은 건너뛰기로 했다. 임상 1상은 주로 약의 안전성(독성)을 본다. 혈장 치료제의 경우 환자 몸 속의 혈장을 기반으로 개발하기에 독성에는 큰 문제가 없다고 평가된다.
GC녹십자는 식약처 승인을 받은 대로 5개 병원에서 환자 60명을 대상으로 혈장 치료제의 안전성과 유효성 확인에 나선다. 임상 참여 병원은 서울아산병원·삼성서울병원·중앙대병원·고대안산병원·충남대병원 등 5개 병원이다.
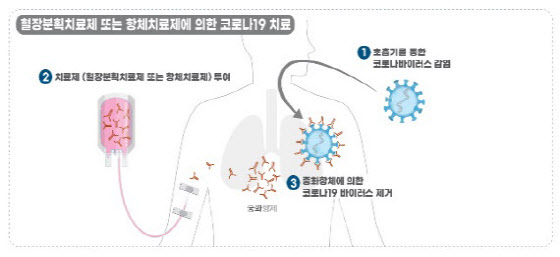
혈장 치료제는 코로나19 회복기 환자 혈장에서 항체가 들어 있는 면역 단백질만 걸러내 고농도로 농축해 만든 의약품이다. 회복기 환자 혈장을 중증 환자에 직접 헌혈하듯 투여하는 ‘혈장 치료’와는 다른 것이다. 혈장은 혈액 구성 요소 중 적혈구·백혈구·혈소판이 빠진 누런빛의 액체 성분이다.
GC녹십자는 혈장 치료제 개발의 관건인 완치자의 혈액 확보에서도 일정부분 성과를 낸 상태다. 회사에 따르면 18일 기준 혈장 공여 신청자는 1184명이며 이 가운데 채혈자는 881명이다. 완치자 1명에서 기증받은 혈장으로는 코로나19 환자 0.3~0.5명에 사용할 수 있는 혈장 치료제를 만들 수 있다. 대략 300~400명 분량의 혈장이 확보된 셈이다.
하지만 이달 24일부터는 수도권과 강원도 등 헌혈의 집 21곳에서, 내달 7일부터는 충청도, 전라도, 경상도 헌혈의 집 25곳에서도 코로나19 완치자 혈장 채혈이 가능하다.
김신우 경북대 감염내과 교수는 “임상 2상의 경우 임상시험에 동의한 환자를 얼마나 빨리 확보하느냐가 관건일 것”이라며 “임상 2상은 빨라도 2~3개월은 걸릴 것”이라고 말했다. 정부는 코로나19 혈장 치료제의 경우 올해 안에 품목허가 승인을 목표로 하고 있다. GC녹십자는 혈장치료제를 질병관리본부 산하 국립보건연구원과 공동 개발 중이다.
|










![[포토] 이재경 '핀하이로 쏜다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400197t.jpg)
![[포토] 축시 낭독](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400720t.jpg)
![[포토] 2024 세계한인회장대회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400598t.jpg)
![[포토]유현조,나이스 마무리 퍼트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400048t.jpg)
![[포토]박도은,핀 공략을 생각한다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300270t.jpg)
![[포토]"예쁜 피부는 역시" 엘렌실라, W페스타 부스 운영](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300485t.jpg)
![[포토]전국 의대 교수, '의평원 무력화 막을 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300350t.jpg)
![[포토]부천국제만화축제 참가한 부천대학교 학생들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300332t.jpg)
![[포토]파란하늘과 가을 꽃](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300310t.jpg)
![[포토]개천절 경축식 만세삼창](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300275t.jpg)

![[포토]임희정,최종일 우승 향한 미소](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100700308t.jpg)


