|
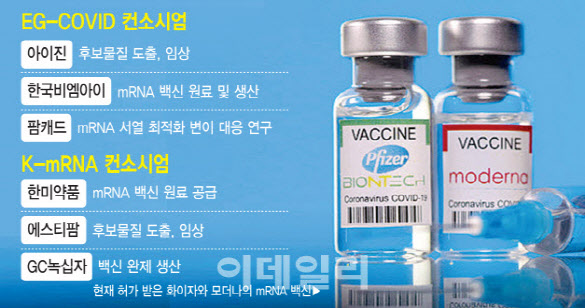
6일 mRNA 코로나19 백신을 개발하기 위해 한미약품(128940), 에스티팜, GC녹십자(006280)가 손을 잡은 K-mRNA 컨소시엄의 한 관계자는 임상 3상 방식에 대해 “모더나나 화이자 백신에 견주는 비교임상을 고려하고 있다”며 “7000억원 중 900억원 정도가 임상 비용으로 책정된 것으로 알고 있다”고 말했다. 이 관계자는 “900억원에는 임상 1·2·3상이 모두 포함된 것”이라며 “일반임상은 피험자 모집도 어려운 데다 수만명 모집에 수천억원이 필요해 국내 기업이 감당하기 불가능하다”고 설명했다.
앞서 3사가 주축을 이룬 K-mRNA 컨소시엄이 지난달 29일 출범됐다. 3사는 내년 상반기 중 mRNA 코로나19 백신을 개발할 목표를 내걸으면서 임상과 핵심 원료, 대량생산설비 구축에 7000억원 이상을 투자할 계획이라고 밝혔다. 아이진이 주도하고 한국비엠아이, 팜캐드가 참여하는 또다른 토종 mRNA 백신 개발 컨소시엄(EG-COVID)도 비교임상 방식의 임상 3상을 고려 중이다. EG-COVID 컨소시엄 한 관계자는 “결정된 건 아니지만, 비교임상을 할 수 있으면 좋겠다”며 “모더나나 화이자와 비교하는 게 가장 유력하다”고 했다.
두 컨소시엄에서는 적어도 미국과 유럽 등을 제외한 아시아나 남미 등에서는 비교임상을 거친 백신이라도 수출이 가능할 것이라는 의견이 나왔다. EG-COVID 컨소시엄 한 관계자는 “일단 남미나 동남아시아 등에서는 비교임상이 수출에 큰 영향을 주지는 않을 것이라고 본다”며 “백신에서 제일 중요한 게 안전성인데 1상에서 안전성이 담보된다면 효능 부분은 비교임상을 통해 견줘볼 수 있을 것”이라고 말했다. K-mRNA 컨소시엄 관계자는 “국내와 동남아시아 일부에서 비교임상도 인정받을 수 있을 것”이라면서도 “선진국 수출은 쉽지 않을 거 같다”고 했다.
업계 관계자는 “백신 개발 성공은 임상 성공에서 끝나는 게 아니라 판매까지 이어져야 빛을 발할 수 있다”며 “비교임상 등의 임상 방식이나 사용하는 기술의 지식재산권 문제 등도 잘 살펴야 한다”고 말했다.






![[포토]박종준 처장, 특수공무집행방해 혐의로 경찰 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011000511t.jpg)
![[포토] 맘스홀릭베이비페어 전시](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010901108t.jpg)
![[포토]수도권 첫 한파주의보](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010901027t.jpg)
![[포토]'무죄'받고 이동하는 박정훈 전 수사단장](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900998t.jpg)
![[포토]기자회견 하는 김상욱 의원](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900987t.jpg)
![[포토]전국정당을 넘어 K-정당으로 향하는 더불어민주당](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900948t.jpg)
![[포토]발언하는 권영세 위원장](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900599t.jpg)
![[포토]포즈 취하는 팀테일러메이드](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010800134t.jpg)
![[포토]서울 올겨울 첫 한파특보… 내일 체감온도 영하 17도](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010800820t.jpg)


![[포토]홍재경 아나운서,론칭쇼 진행합니다](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25010800229h.jpg)
![공중제비 도는 로봇개 “어메이징”…로봇 공습 나선 中[영상][CES2025]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25011000623b.jpg)