|
항암치료를 위해 암 세포에만 약물이 전달되는 표적 전달체용 나노입자의 개발은 상당히 까다롭다. 그 이유는 나노입자가 몸 안에 주입되면 예측하기 힘든 다양한 생체 내 장애물로 인해 암 세포까지 도달하지 못해 기대만큼의 항암효과를 보지 못하기 때문이다. 현재까지 나노입자의 암 조직 도달량은 주입량 대비 평균 0.7% 정도에 불과한 실정이다.
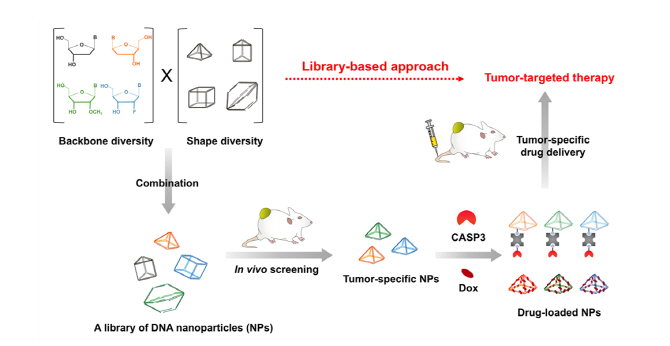
이 문제를 해결하기 위해서는 다양한 나노입자를 한꺼번에 설계·제조해 나노입자 라이브러리를 구축한 뒤 모든 방해요소를 극복하고 암 세포에만 많이 도달하는 최적의 나노입자를 동물 모델 실험을 통해 선별하는 방법이 필요하다.
KIST 안대로 박사팀은 1나노미터(nm, 10억분의 1m) 이하 수준으로 정밀하게 크기 및 모양 제어가 가능한 DNA 염기서열 기반 나노 구조체를 약물 전달체로 활용했다. DNA는 생명 분자로 잘 알려져 있지만 염기 서열을 분자설계 코드로 활용하면 다른 소재로는 불가능한 다양한 형태와 크기의 나노구조체를 매우 정밀하게 조절해 만들 수 있다. 연구팀은 다양한 DNA 종류와 서열 순서를 조합해 모양과 화학적 성분이 다른 여러 개의 나노입자로 구성되는 라이브러리를 구축했다.
또 안대로 박사팀은 이렇게 구축한 DNA 나노입자 라이브러리를 동물 모델에서 검색해 기존에 보고된 다른 암표적성 나노입자보다 약 3배 이상의 전달률을 보이는 고성능 암 표적 전달체 3종을 발굴하는 데 성공했다. 발굴된 전달체에 저분자 항암제 및 단백질 항암 약물을 탑재해 암 질환 동물 모델에 주입했을 때 다른 장기에는 손상을 주지 않고 암 조직에만 선택적으로 약물이 도달해 높은 항암 효능을 보였다.
이 연구는 과학기술정보통신부 지원으로 KIST 기관고유사업과 한국연구재단 미래유망융합파이오니아사업 및 방사선기술개발사업으로 수행됐으며 연구 결과는 ‘바이오머티리얼스(Biomaterials)’ 최신호에 온라인 게재됐다.








![[포토]우정사업본부, 2025 연하우표 발행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120200431t.jpg)
![[포토]비상의원총회, '대화하는 추경호-조정훈'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120200384t.jpg)
![[포토]최상목 "野 감액안 허술한 예산…무책임 단독 처리 깊은 유감"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120200344t.jpg)


![[포토]12월 LPG 국내 프로판 가격 인상](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120100332t.jpg)
![[포토]초코과자 가격 상승](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120100324t.jpg)
![[포토]점등 앞둔 사랑의 온도탑](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120100312t.jpg)
![[포토]박찬대 “감액 예산안, 법정시한인 내일 본회의 상정”](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120100294t.jpg)
![[포토]짙은 안개에 갇힌 도심](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120100227t.jpg)



![삼성전자, 4거래일 연속 하락…5만3000원대 사수 안간힘[특징주]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24120200408h.jpg)
