|
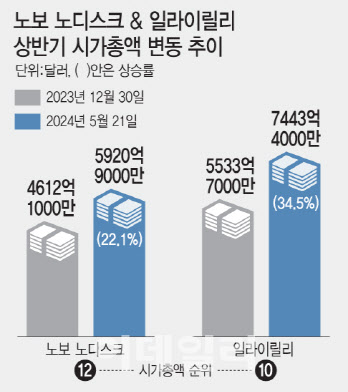
특히 일라이릴리 시총은 지난해 12월 말(5533억 달러) 대비 34.5%가량 큰 폭으로 상승했다. 노보 노디스크 역시 같은 기간 약 22.1% 상승한 것으로 확인됐다. 이들의 시총 상승 랠리를 이끈 주요 원인으로는 비만약의 상업화 성공 및 적응증 확장 성과 등이 꼽힌다.
실제로 일라이릴리는 지난해 12월 말 ‘젭바운드’(성분명 티르제 파타이드)를 미국에서 처음 출시했다. 지난 2월 회사는 해당 물질에 대해 대사이상지방간염(MASH) 관련 글로벌 임상 2상에 성공했다는 발표도 내놓았다. 젭바운드는 지난 1분기 동안 5억1700만 달러(한화 약 7000억원)의 매출을 올렸다.
노보노디스크는 지난 2월 ‘위고비’(성분명 세마글루타이드)의 지난해 매출이 313억4300만 크로네(한화 약 6조원)을 달성했다고 밝히면서 주목받았다. 위고비는 주1회 주사하는 최초의 비만약이다. 한달 뒤인 3월에는 미국 식품의약국(FDA)이 과체중 또는 비만인 성인 심혈관 질환자의 심장마비나 뇌졸중을 예방하는 용도로 위고비의 적응증 확대를 승인하기도 했다.
|
앞서 언급한 것처럼 일라이릴리와 노보 노디스크는 모두 비만약의 적응증 및 시장 확대, 경구제 개발, 타질환 신약 개발 등을 병행하고 있다.
이중 도나네맙의 승인 결론에 대한 관심이 큰 축을 형성하고 있다. 일라이릴리는 당초 지난 3월 도나네맙의 승인을 점쳤지만, 당시 FDA가 한번 더 안전성과 효능을 논의하기 위해 그 최종 결정을 연기한 바 있다. 도나네맙의 임상 참여 환자 중 3.7%에서 뇌부종과 미세 출혈이 발생했으며, 임상 과정에 참여했다가 사망한 환자도 나왔기 때문이다.
치매 신약 개발에 정통한 한 연구자는 “현재 쓰는 레켐비의 뇌부종 부작용 비율도 약 10%다. 하지만 임상에서 사망사례가 없었던 점이 도나네맙과 다르다”며 “안전성을 따져봐야겠지만 도나네맙의 임상에서 인지기능 개선효과가 35%로 레켐비(27%)를 능가했던 만큼 시장의 기대가 큰 물질이다”고 설명했다. 도나네맙의 승인 결정이 긍정적으로 이뤄진다면 릴리의 시총이 한 차원 더 상승할 수 있을 전망에 힘이 실리는 이유다.
노보노디스크에 대해서는 연내 △위고비의 중국 승인 여부 △MASH 적응증 2상 재분석 결론 △위고비 성분의 경구 버전 후기 3상 진행 등에 대한 이슈에 주목할 만하다. 특히 미국에 이어 두 번째로 큰 중국시장에서 현재 위고비가 연내 승인될 경우 그 매출 확장성에도 가속도가 붙을 전망이다. 한편 지난 2월 일부 지표를 미충족했던 위고비의 MASH 임상 2상에 대한 재분석 결과가 나올 시점도 다가오고 있어, 노보 노디스크의 시총 상승세의 변곡점으로 작용할 수 있다는 분석이 나온다.










![[포토] 원·달러 환율 오를까?](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900849t.jpg)
![[포토] 폭설 피해](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900576t.jpg)
![[포토] 주식시장 활성화 테스크포스-경제계 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900547t.jpg)
![[포토]최재해, '정치적 탄핵 매우 유감...자진 사퇴 생각 없다'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900431t.jpg)
![[포토]'모두발언하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900370t.jpg)
![[포토]이데일리 퓨처스포럼 송년회 무대](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801622t.jpg)
![[포토]용산국제업무지구 개발계획 공동협약식에서 협약서 서명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801123t.jpg)

![세단 주행감 갖춘 SUV…더 진화한 패밀리카 'BMW 뉴 X3'[타봤어요]](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24113000092h.jpg)
![“오늘은 회사 안 갈래”…출퇴근 자유로운 ‘이 회사’[복지좋소]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24113000047b.jpg)

