14일 제약·바이오 업계에 따르면 휴미라는 지난해 글로벌 1위 매출을 기록할 것으로 예상된다. 유럽 시장에서는 바이오시밀러와의 경쟁으로 고전하고 있지만, 미국 매출이 증가하면서 207억 달러(약 24조9580억원)라는 사상 최대 매출을 기록했다. 2020년 MSD 키트루다가 144억 달러(야구 17조2742억원)였던 점을 고려하면 2021년 역시 휴미라가 매출 1위를 차지할 전망이다.
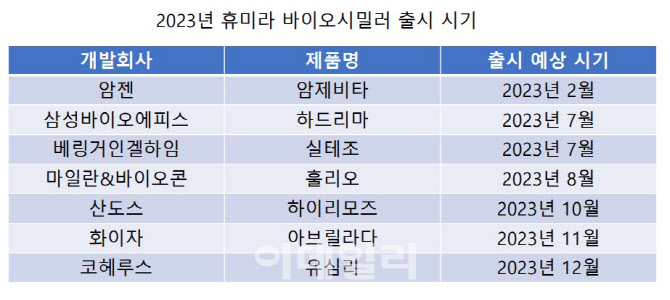
휴미라는 2012년부터 10년동안 매출 1위 자리를 유지하고 있지만, 문제는 미국 내 특허가 만료되는 내년이다. 2018년 특허가 풀린 유럽 시장과 다르게 미국 시장은 내년부터 특허가 풀린다. 내년 출시를 계획하고 있는 바이오시밀러만 7개에 달한다. 삼성바이오에피스를 비롯해 암젠, 마일란, 베링거인겔하임, 화이자, 코헤루스, 산도스가 출시를 준비하고 있다. 업계는 내년 바이오시밀러가 출시되면 휴미라 매출이 직격탄을 맞을 것으로 예상한다. 릭 곤잘레스 애브비 CEO도 지난 3일 실적발표와 함께 “휴미라 매출이 2023년부터 최대 55% 타격을 받을 수 있다”고 언급했다.
|
삼성바이오에피스는 휴미라 바이오시밀러인 임랄디를 암젠 등과 같이 가장 먼저 유럽에 출시했는데, 미국에서는 암젠이 개발한 암제비타가 퍼스트무버가 될 가능성이 높다. 암젠은 내년 1분기 암젠비타를 미국 시장에 출시할 계획이다. 이는 애브비와 암젠 측의 특허 만료에 따른 제품 출시 계약에 따른 것이다. 삼성바이오에피스가 개발한 하드리마는 암젠에 이어 두 번째로 미국 시장에 출시될 것으로 보인다. 퍼스트무버가 아님에도 삼성 측은 바이오시밀러 경쟁에서 자신감을 내비치고 있다.
삼성바이오에피스는 고농도 제품 출시로 전략을 변경한 상태다. 저농도 제품은 이미 개발을 완료하고 미국 식품의약국 허가를 받았지만, 최근 휴미라가 저농도에서 고농도 제품으로 변경되면서 현장 니즈가 크다는 것이 확인되자 고농도 제품 개발로 방향을 선회했다. 적응증이 많은 자가면역질환은 저농도 제품의 경우 환자가 하루에 여러번 주사를 맞아야 하는 경우가 많아, 1회 주사가 가능한 고농도 제품에 대한 환자 니즈가 크다는 게 업계 설명이다. 저농도 제품을 먼저 출시 후 고농도 제품을 선보일 계획이다.
삼성바이오에피스 관계자는 “하드리마는 현재 고농도 제품 출시를 위해 임상 완료하고, 허가 신청을 한 상태다. 기존 저농도 제품이 허가를 받은 만큼 임상 1상 데이터로만 변경 허가가 가능하다”며 “애브비와의 협의로 암젠 제품이 먼저 출시되지만, 미국 시장은 제형, 약가정책, 보험 등 다양한 변수들이 시장 점유율에 영향을 미친다. 고농도 외 또 다른 전략도 검토하고 있다”고 말했다.
삼성바이오에피스가 검토하고 있는 휴미라 바이오시밀러 전략은 인터체인저블 시밀러 개발이다. 인터체인저블 시밀러는 처방받은 오리지널약을 별도 스위칭 처방전 없이도 약국에서 대체 처방이 가능한 제품이다. 이를 위해서는 유효성과 안전성 등 오리지널약과 동일한 임상 결과를 입증해야 한다. 또한 오리지널약과 바이오시밀러를 교차 사용할 때 안전성과 유효성 감소에 대한 위험성도 평가해야 한다.
바이오시밀러 업계는 미국이 교체처방을 허용하고, FDA가 지난해 7월 마일란이 개발한 당뇨병 치료 바이오시밀러 셈글리를 인터체인저블 바이오시밀러로 허가한 것이 주목하고 있다. 의사가 휴미라를 처방하더라도 약국에서 하드리마로 대체처방이 가능해 오리지널 의약품 점유율을 가지고 올 수 있는 새로운 기회가 열리는 셈이다. 삼성바이오에피스 관계자는 “글로벌 바이오시밀러 업계는 오리지널 제품의 대체 처방이 가능한 인터체인저블 제품이 시장 점유율을 확대할 기회라고 인식하고 있다”며 “베링거인겔하임 제품이 인터체인저블 제품으로 허가를 받았다. 휴미라와 타 바이오시밀러 제품과의 경쟁에서 우위를 점하기 위해 고농도 전략과 함께 인터체인저블 제품을 개발해 대응할 것”이라고 강조했다.








![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]영화 속 배경에서 찰칵](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901369t.jpg)
![[포토] 아수라장된 기자회견장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901115t.jpg)
![[포토]다양한 식음료가 한 자리에, '컬리 푸드페스타 2024'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900958t.jpg)
![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)



