|
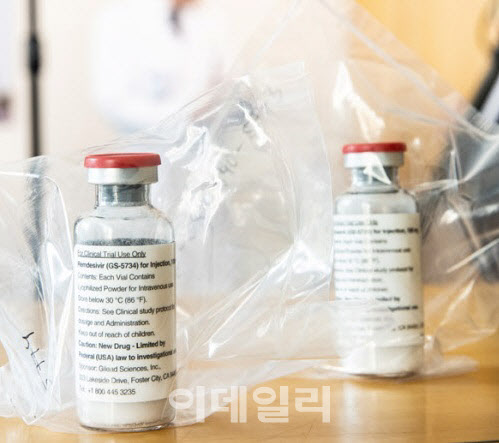
식품의약품안전처는 코로나19 치료제로 개발 중인 항바이러스제 렘데시비르에 대해 특례수입을 결정했다고 3일 밝혔다.
이에 따라 질병관리본부는 식약처 등 관계부처, 수입자인 길리어드사이언스코리아와 조속한 국내 수입을 협의해 나갈 예정이다.
식약처는 렘데시비르가 중증의 입원 환자에 효능·효과가 있다고 설명했다.
구체적 대상은 △실내공기에서 산소포화도 94% 이하인 환자 △보조산소 치료가 필요한 환자 △비침습적 또는 침습적 기계환기나 체외막산소요법(ECMO)이 필요한 환자 등이다.
앞서 질병관리본부는 ‘신종감염병 중앙임상위원회’가 코로나19 치료제로서 렘데시비르의 국내 도입을 제안하면서 식약처에 특례수입을 요청했다.
식약처는 특례수입 결정 배경에 대해 “렘데시비르 사용에 따른 중증환자에서의 치료기간 단축은 임상적으로 의미가 있고 선택 가능한 치료제의 추가적인 확보가 필요하다”고 설명했다.
또한 현재 미국, 일본, 영국에서도 렘데시비르를 코로나19 팬데믹 상황에서 사용하도록 한 점도 고려했다고 덧붙였다.
정부는 국내 수입자인 길리어드사이언스코리아와 함께 렘데시비르를 빠른 시일 내에 수입할 수 있도록 최대한 지원해 나갈 방침이다.
렘데시비어는 신종 인플루엔자 치료제 ‘타미플루’를 개발한 미국 제약업체 길리어드 사이언스가 또 다른 전염병인 에볼라 치료제로 개발하던 약물이다. 이 약품은 사람 세포 속에 들어온 코로나19 바이러스의 증식을 멈추는 기능을 하는 것으로 알려졌다.
앞서 미국 국립보건원(NIH)은 이 약물이 코로나19 환자의 회복 기간을 15일에서 11일로 단축할 수 있다는 연구 결과를 보고한 바 있다. 사망률의 경우 렘데시비어를 투약한 실험군이 약 7%, 그렇지 않은 비교군이 약 12%였다.







![[포토]메리크리스마스](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400797t.jpg)
![[포토]즐거운 눈썰매](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400779t.jpg)
![[포토]취약계층 금융 부담 완화, '인사말하는 이재연 원장'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400633t.jpg)
![[포토]국민의힘 의원총회, '모두발언하는 권성동 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400506t.jpg)
![[포토]윤석열 대통령 탄핵심판 첫 변론 준비기일 27일 예정대로 진행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400433t.jpg)
![[포토]'더불어민주당 원내대책회의'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400387t.jpg)
![[포토]국무회의 입장하는 한덕수 권한대행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400378t.jpg)
![[포토]은행권 소상공인 금융지원 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300609t.jpg)
![[포토]인사청문회 출석한 마은혁 헌법재판관 후보자](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300404t.jpg)
![[포토]아침 영하 10도, 꽁꽁 얼어붙은 도심](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300843t.jpg)




