이 진단키트는 지난 8월 23일 식품의약품안전처로부터 체외진단의료기기(3등급)로 허가받아 국내 요양급여 대상으로 결정됐고 건강보험 수가도 책정돼 국내 판매 절차를 모두 마쳤다. 이번에 CE 인증을 받음으로써 유럽 시장 판매가 가능해졌다.
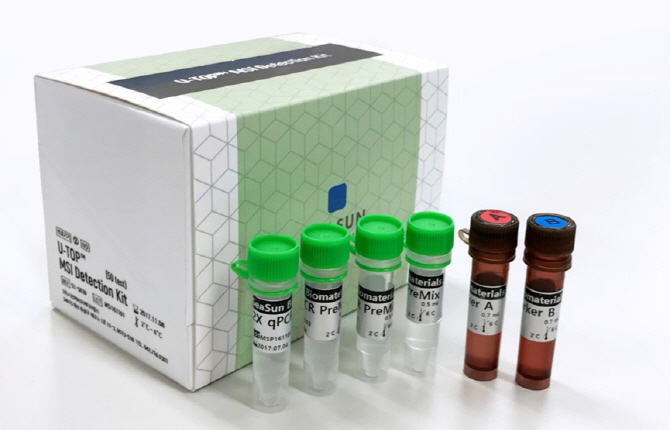
유톱 MSI 진단키트는 실시간중합효소연쇄반응을 통해 현미부수체 불안정성을 진단하는 세계 최초의 제품으로 한번의 PCR 반응만으로 현미부수체 불안정성을 진단해낼 수 있다. 유전자 증폭 후 길이를 측정하는 기존 절편분석 기법은 여러 단계를 거쳐야 하지만, 이 진단키트는 DNA 염기서열의 길이 변화를 온도 변화로 감지하는 기술을 적용해 한번에 검사가 가능한 고민감도를 구현한 게 가장 큰 장점이다. 검사에 필요한 시간과 비용이 대폭 절감된 것.
지난 5월 미국 식품의약국(FDA)이 미국 머크사의 ‘키트루다’(성분명 펨브롤리주맙)를 암의 발생 부위에 관계없이 현미부수체불안정성을 가지는 암 환자에게 처방할 수 있도록 세계 최초로 허가 승인하면서 현미부수체불안정성 진단키트의 시장성도 부각됐다, 이에 시선바이오는 식약처 허가 및 유럽 CE 인증 등을 신속하게 통과해 전무했던 이 분야 진단키트 시장에 선도적인 입지를 차지하게 됐다. 국내서는 대장암의 보조진단을 적응증으로, 유럽 등 해외에서는 맞춤형 항암치료에 면역항암제를 적용할 수 있는지 여부를 판가름하는 바이오마커 진단 용도로 판로가 마련된 셈이다.
|







![[포토] 맘스홀릭베이비페어 전시](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010901108t.jpg)
![[포토]수도권 첫 한파주의보](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010901027t.jpg)
![[포토]'무죄'받고 이동하는 박정훈 전 수사단장](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900998t.jpg)
![[포토]기자회견 하는 김상욱 의원](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900987t.jpg)
![[포토]전국정당을 넘어 K-정당으로 향하는 더불어민주당](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900948t.jpg)
![[포토]발언하는 권영세 위원장](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010900599t.jpg)
![[포토]포즈 취하는 팀테일러메이드](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010800134t.jpg)
![[포토]서울 올겨울 첫 한파특보… 내일 체감온도 영하 17도](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010800820t.jpg)

![[포토] 김혜수, 나홀로 화보](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010800074t.jpg)

![[포토]홍재경 아나운서,론칭쇼 진행합니다](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25010800229h.jpg)


