한국생명공학연구원은 위해요소감지BNT연구단 이규선 박사(공동 제1저자)와 한국기초과학지원연구원 이성수 박사(공동 제1저자)가 스탠포드 의과대학과 공동으로 미토콘드리아의 세포 내 특정 단백질의 변화가 칼슘을 조절해 신경줄기세포의 유지와 세포분열에 영향을 끼친다는 사실을 규명했다고 27일 밝혔다.
세포 내 대표적 소기관인 미토콘드리아는 영양분으로 흡수된 포도당으로부터 해당 과정과 산화적 인산화 과정을 통해 세포의 주요 에너지원인 ATP(아데노신삼인산, adenosine triphosphate)를 생성하는 발전소와 같은 역할을 수행한다.
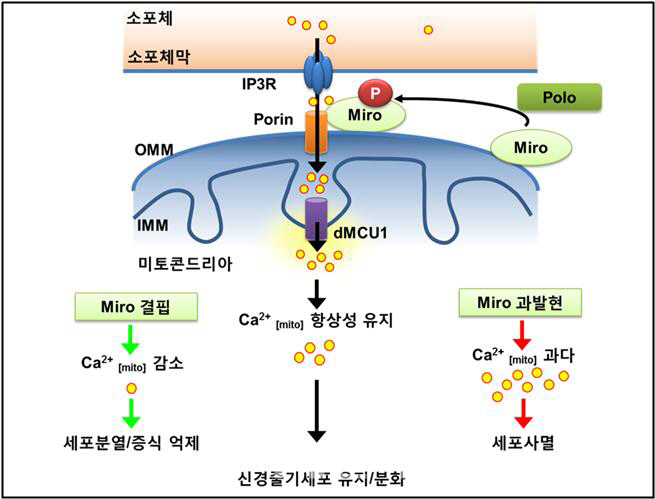
또 미토콘드리아는 세포 내 칼슘 농도 항상성에 관여하는 소기관으로 주목받고 있으며, 세포 내 칼슘의 주요 저장고인 소포체(endoplasmic reticulum)와 상호작용을 통해 칼슘을 흡수해 세포 에너지 대사 활성 및 세포사멸을 조절한다.
미토콘드리아의 칼슘이 부족해지면 ATP 생성이 감소해 세포의 생명 유지 기능이 저하된다.
이에 따라 미토콘드리아의 기능 이상은 대사질환, 신경퇴행성질환, 근골격계질환 등 다양한 질환의 원인이 될 뿐만 아니라 노화 촉진의 주요한 원인으로 알려졌다.
특히 줄기세포 및 암세포는 정상세포에 비해 활발한 세포 증식을 유지하기 위해 많은 양의 에너지를 필요로 하며, 에너지 대사 재조정(metabolic re-programing)을 통해 미토콘드리아의 활성을 조절한다.
이는 미토콘드리아에 의한 에너지 대사조절 기능을 통한 질환 극복을 위해 세포소기관 간의 상호 작용에 의한 미토콘드리아의 칼슘 항상성 조절 기전이 주목받고 있는 이유다.
또 미토콘드리아 칼슘 농도에 따라서 신경줄기세포의 자가재생산(self-renewal) 활성이 조절되는 것을 알아냈다.
이 박사는 “이번 연구 성과는 신경암 및 신경퇴행성질환을 효과적으로 치료하기 위해서는 미토콘드리아의 칼슘 항상성을 조절하는 것이 중요하다는 사실을 밝힌 것”이라며 “새롭게 규명된 Polo-Miro 단백질의 상호작용을 통해 조절되는 미토콘드리아 칼슘 조절 기전과 이에 연관된 다양한 칼슘 조절 인자들을 동시에 표적으로 하는 신약 개발은 효율적 암 치료제뿐만 아니라 신경퇴행성질환, 염증 질환, 심혈관 질환, 근육노화 및 노인성 관련 질환 등의 치료제 개발에도 큰 기여를 할 것으로 기대된다”고 설명했다.
한편 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 바이오의료기술개발사업의 지원으로 수행됐으며, 생물학 분야의 세계적 저널인 Cell지의 자매지 ‘Developmental Cell(IF 10.366)’ 18일자 온라인 판에 게재됐다.
|
|








![[포토]골프존 파스텔 합창단,지역주민위한 공연](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400127t.jpg)
![[포토]'규탄사하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120401162t.jpg)
![[포토]비상계엄 해제 후 한자리에 모인 한덕수 총리와 국무위원들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120401092t.jpg)
![[포토]최상목 경제부총리, '어두운 표정'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400960t.jpg)
![[포토]청사들어서는 한덕수 총리](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400786t.jpg)
![[포토] 대통령실 입구의 취재진](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400817t.jpg)
![[포토]'긴급 의원총회 참석하는 추경호 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400571t.jpg)
![[포토]'긴박했던 흔적들'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400485t.jpg)
![[포토]조국, '국가 비상사태 만든 이는 尹...탄핵해야'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400366t.jpg)
![[포토]尹, '비상 계엄 해제할 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400277t.jpg)




