미래창조과학부(장관 최양희)는 암을 유발하는 대표적인 인자인 베타카테닌과 라스 단백질을 동시에 분해해 암세포를 억제하는 혁신형 저분자 화합물 대장암 치료제를 개발했다고 22일 밝혔다.
최강열 교수팀(연세대학교)이 주도한 이번 연구는 미래창조과학부 기초연구사업(집단연구)의 지원을 받아 진행됐고 이번 연구 결과는 화학생물학 분야의 저명한 학술지 ‘네이처 케미컬 바이올로지 (Nature Chemical Biology)’에 14일 온라인판에 게재됐다.
대장암은 높은 빈도로 발병하는 암으로 현대사회의 암 사망원인의 주요 원인으로 꼽히고 있다. 현재 사용 중인 치료제들은 지속적 사용에 따라 내성과 저항성을 보여 이를 극복하기 위한 효과적 치료법의 개발이 요구되고 있다.
대장암은 APC와 KRas 돌연변이를 포함한 유전적 변이에 의해서 발생 하는데, 이들 돌연변이로 인해 많은 암환자들에게서 윈트·베타카테닌 및 라스 신호전달체계의 비정상적인 활성화가 관찰된다.
연구팀은 선행연구를 통해 윈트·베타카테닌 신호전달계의 신호전달 억제를 통해서 라스 단백질이 분해될 수 있음을 규명했다.
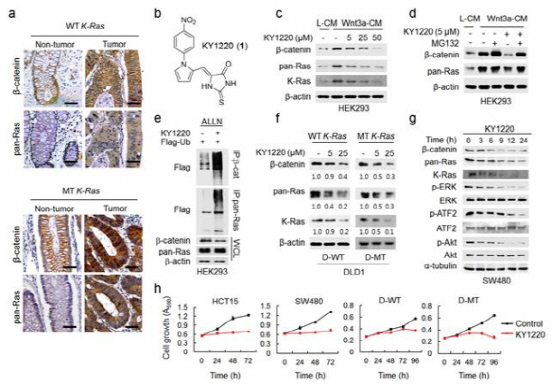
이를 바탕으로 저분자 화합물 라이브러리를 검색해 윈트·베타카테닌 신호전달계 억제를 통한 베타카테닌과 라스 단백질을 동시 분해 가능한 화합물을 발굴했다.
또한 유도체 합성을 통해 발굴한 물질보다 물성 및 효능이 증진된 화합물 (KYA1797K)을 확보하고, 화합물이 돌연변이를 가진 다양한 대장암 세포의 성장 및 변화(transformation)를 억제함을 세포 수준 및 동물실험 수준에서 확인했다.
이번 연구의 베타카테닌과 라스 단백질을 동시에 분해하는 저분자 화합물 및 치료 전략은 대장암을 비롯한 신호 전달계가 과활성화 돼있는 다양한 암에 적용할 수 있는 다중표적 항암제 개발에 적용할 수 있다. 또한 라스를 제어하는 항암제 개발에 신규 전략이 될 수 있을 것으로 기대된다.
최강열 교수는“베타카테닌과 라스 단백질을 동시에 분해하는 것이 윈트·베타카테닌 및 라스 신호전달체계가 과활성화 돼있는 대장암과 다양한 암을 치료하는 다중표적 항암제 개발의 새로운 전략임을 보여줬다”며 “특히 라스 치료용 혁신형 항암제의 개발 가능성을 제시하였다”고 밝혔다.
|








![[포토]코스피-코스닥 동반 상승 마감](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300908t.jpg)
![[포토]따스한 온기를 퍼지는 행복촌](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300829t.jpg)
![[포토]이웃을 위한 연탄나눔봉사활동](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300804t.jpg)
![[포토]한동훈, '여성의 힘으로 세상을 바꾸자'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300792t.jpg)
![[포토]설영희부띠끄 24W/25S 살롱 패션쇼](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300633t.jpg)
![[포토]유승민 "대한체육회장 공식 출마합니다"](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300064t.jpg)
![[포토]더불어민주당 원내대책회의](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300465t.jpg)
![[포토]'모두발언하는 추경호 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300359t.jpg)

![[포토]의정갈등에 피해는 환자에게…](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120200764t.jpg)



![[단독]공정위, 中 '알테쉬' 제재 절차 밟는다…과징금 규모는](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24120300940h.jpg)
