|
미래창조과학부와 한국연구재단은 5일 성균관대 화학고분자공학부 엄숭호 교수 연구팀이 세포 내 핵의 기능이 저하된 경우, 인공 세포핵 시스템으로 대체할 수 있는 가능성을 제안하는 연구를 발표했다고 밝혔다.
연구결과는 나노생명과학분야의 권위 있는 학술지인 스몰(Small) 온라인판 8월 27일 자에 게재됐다.
다운증후군과 같은 유전 질환을 치료하기 위해서는 정상 유전자를 대상 세포에 전달하는데, 일반적으로 그 전달 효율이 1%미만으로 매우 떨어지고 암과 같은 심각한 부작용의 가능성이 있어 실제 임상 치료에 한계로 지적되고 있다.
이를 극복하기 위해 대상 세포핵으로 직접 유전자를 전달하지 않고 세포핵 이전에 메신저 RNA에서 단백질 발현이 가능하도록 하는 방법이 제시되고 있으나 세포질 내에 빠른 분해로 낮은 효율 등이 한계로 지적되고 있다.
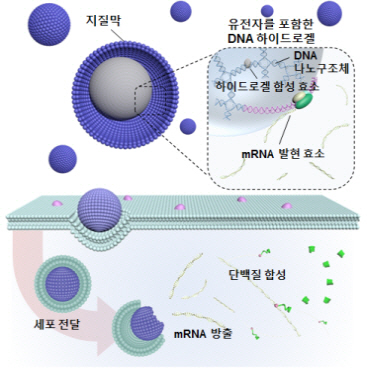
게놈 하이드로겔 시스템이 생체 외에서 단백질 발현인자들과 만났을 때 조밀한 겔 세망조직 내에서 발현 인자들의 잔류효과가 극대화돼 수백 배 이상의 단백질 생산 효율을 보였으며, 16가지 이상의 기능성 단백질들도 쉽게 생산됐다.
입자형태로 제작된 게놈 하이드로겔의 표면을 세포 막 투과가 용이하도록 지질막으로 코팅해 세포 핵 모사 시스템, 즉 인공 세포핵을 완성했다.
단백질 생산 공정기술과 접목해 세포핵 입자들을 플랜트화 할 수 있다면 특정 단백질군들을 대량배양 할 수 있어 다양한 단백질 치료제 생산능력의 향상에 크게 기여할 것으로 예상된다.
엄숭호 교수는 “이번 연구를 통해서 기존의 효율이 낮은 유전자 이입 기술에 대응하는 새로운 첨단 치료기술을 제안한 것은 인류의 고질적인 유전 질환을 정복할 수 있는 토대를 마련한 것으로 볼 수 있다”고 말했다.
|









![[포토]코스피-코스닥 동반 상승 마감](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300908t.jpg)
![[포토]따스한 온기를 퍼지는 행복촌](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300829t.jpg)
![[포토]이웃을 위한 연탄나눔봉사활동](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300804t.jpg)
![[포토]한동훈, '여성의 힘으로 세상을 바꾸자'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300792t.jpg)
![[포토]설영희부띠끄 24W/25S 살롱 패션쇼](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300633t.jpg)
![[포토]유승민 "대한체육회장 공식 출마합니다"](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300064t.jpg)
![[포토]더불어민주당 원내대책회의](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300465t.jpg)
![[포토]'모두발언하는 추경호 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300359t.jpg)

![[포토]의정갈등에 피해는 환자에게…](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120200764t.jpg)




