|
식품의약품안전처는 한국화이자제약의 ‘코미나티주’에 대한 안전성과 효과성을 자문하기 위해 25일 진행한 ‘중앙약사심의위원회’ 회의 결과를 이 같이 26일 밝혔다.
검증 자문단은 코로나19 백신 허가를 위한 외부 전문가 ‘3중’ 자문회의 가운데 두번째 단계다. 이번 회의에는 외부 전문가 19인과 식약처 내부 인원 8인이 참석했다.
중앙약심은 코미나티주의 안전성·효과성 인정 여부를 논의한 결과 “품목허가 할 수 있을 것으로 자문했다”고 밝혔다. 또 화이자 백신을 “16세 이상을 대상으로 허가하는 것이 타당하다”고 봤다.
식약처는 이후 마지막 전문가 자문 단계인 ‘최종점검위원회’를 개최해 화이자 백신의 허가 여부를 최종 결정할 예정이다. 식약처는 최종점검위원회 개최일을 밝히지는 않았다.
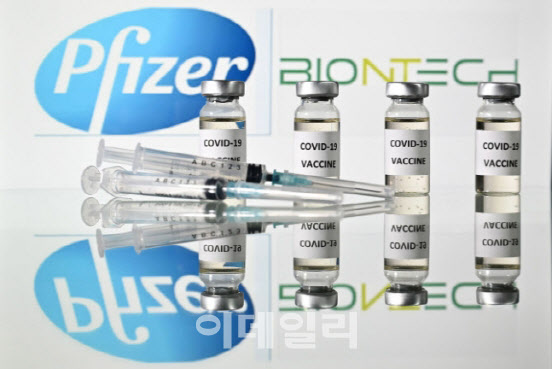
화이자 백신은 바이러스의 유전정보가 담긴 메신저 리보핵산(mRNA·전령RNA)을 활용해 개발된 백신이다. 국내에 도입될 코로나19 백신 5종 가운데 가장 예방효과가 좋다. 반면 보관 및 유통 시에는 영하 60∼90℃의 초저온 콜드체인이 필요해 보관 등이 까다로운 단점이 있다.
이번 검증 절차는 한국화이자제약이 지난달 25일 코미나티주의 품목허가를 신청한 데 따른 것이다. 이날 국내에 공급돼 오는 27일부터 코로나19 환자 치료병원 종사자를 대상으로 접종하는 화이자 백신 물량과는 별개의 것이다. 이날 공급분은 백신 공동구매 프로젝트인 코백스 퍼실리티를 통해 들어오는 물량이다.









![[포토] 이재경 '핀하이로 쏜다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400197t.jpg)
![[포토] 축시 낭독](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400720t.jpg)
![[포토] 2024 세계한인회장대회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400598t.jpg)
![[포토]유현조,나이스 마무리 퍼트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400048t.jpg)
![[포토]박도은,핀 공략을 생각한다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300270t.jpg)
![[포토]"예쁜 피부는 역시" 엘렌실라, W페스타 부스 운영](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300485t.jpg)
![[포토]전국 의대 교수, '의평원 무력화 막을 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300350t.jpg)
![[포토]부천국제만화축제 참가한 부천대학교 학생들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300332t.jpg)
![[포토]파란하늘과 가을 꽃](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300310t.jpg)
![[포토]개천절 경축식 만세삼창](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300275t.jpg)
![[포토]임희정,최종일 우승 향한 미소](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100700308t.jpg)



