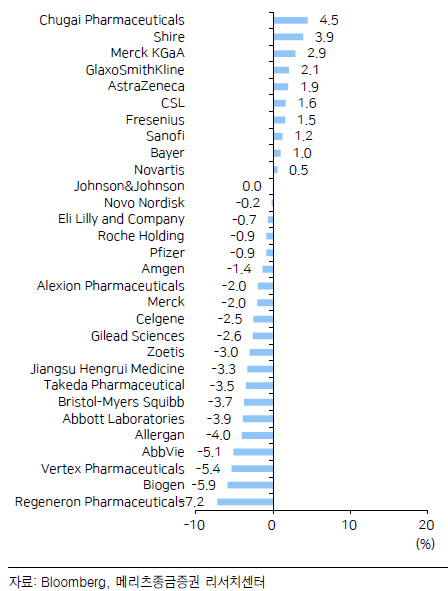
 | | 일주일간 글로벌 제약바이오주 수익률. |
|
[이데일리 이명철 기자] 메리츠종금증권은 임상시험 결과나 미국 식품의약국(FDA) 신약 허가 여부 발표 시점 등을 사전 계산할 수 있다며 신장암 1차 치료제 허가, BTK저해재 임상 3상 중간 결과 발표, 발작성 야간 헤모글로빈뇨증(PNH) 대상 임상 3상 결과 발표 등이 2분기 글로벌 제약·바이오 산업 이슈라고 진단했다.
이태영 메리츠종금증권 연구원은 9일 “데이터를 중심으로 변화해나가는 제약산업 특성상 임상시험의 결과나 FDA의 신약 허가 여부 발표 시점은 기업 실적발표 만큼 중요한 일정”이라며 “대부분 임상 시험에 대한 계획은 미국국립보건원(NIH)을 통해 확인하고 신약의 허가 일정도 전문의약품허가신청자비용부담법(PDUFA)에 의해 사전 계산이 가능하다”고 분석했다.
먼저 PDUFA에 따르면 옵디보(Opdivo)와 여보이(Yervoy)의 신장암 1차 치료제 허가는 4월 16일로 예정됐다. 그는 “다른 면역관문억제제 개발사에서 들려오는 임상 결과가 더욱 좋아 시장 점유율 확대에 대한 기대감은 다소 낮다”며 “로슈가(Roche)가 티센트릭(Tecentriq)과 아바스틴(Avastin)을 병용하는 방법으로 임상을 진행 중인데 효과는 비슷하지만 부작용 측면에서 강점을 보이고 있다”고 설명했다. 그는 또 “현재 해당 분야에서 면역항암제와의 병용요법을 통해 치료방법을 개발하고 있는 국내 기업으로는
신라젠(215600)이 있다”고 전했다.
올해 중순에는 애브비(Abbvie)와 J&J의 핵심 성장동력인 BTK저해제 임브루비카(Imbruvica) 임상 3상 중간 결과 발표가 예정됐다. 결과가 긍정적일 경우 비호지킨 림프종 중에서 가장 흔한 암 중 하나인 DLBCL 시장 진입이 가능하다. 그는 “관련 국내 파이프라인으로는
한미약품(128940)이 일라이 릴리(Eli Lilly)에 기술 이전한 HM71224와
크리스탈(083790)지노믹스가 앱토즈(Aptose)에 기술이전한 CG026806이 있다”며 “HM71224는 개발이 중단된 상황이고 CG026806의 경우 연내 임상시험에 돌입할 예정”이라고 예상했다.
알렉시온(Alexion_이 개발 중인 ALXN-1210은 자사 블록버스터약물인 솔리리스(Soliris)의 타깃 질환인 발작성 야간 헤모글로빈뇨증(PNH) 대상으로 임상 진행 중이다. 이 연구웡는 “ALXN-1210을 2주 1회 투여해야 하는 솔리리스 대비 지속시간이 길어 시장 대체 가능성이 높게 점쳐지고 있는 약물”이라며 “허가 국내 업체인
이수앱지스(086890)는 솔리리스의 바이오시밀러를 개발 중”이라고 전했다.









![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]영화 속 배경에서 찰칵](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901369t.jpg)
![[포토] 아수라장된 기자회견장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901115t.jpg)
![[포토]다양한 식음료가 한 자리에, '컬리 푸드페스타 2024'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900958t.jpg)

![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)


