|
업계에 따르면 수면장애치료제의 전 세계 시장 규모는 약 30억달러(약 3조 4000억원)에 이르며 매년 6~10%씩 성장한다. 업계에서는 재즈의 기술력과 마케팅 능력이라면 수노시가 충분히 승산이 있다고 내다보고 있다. 수노시는 임상시험에서 주간 졸림증 개선 효과가 재즈의 기존 치료제인 ‘자이렘’보다 2배 이상의 효과를 보였다.
수노시는 SK바이오팜에게는 상용화까지 마친 첫 제품이라는데 의의가 있다. SK가 신약개발에 뛰어든 것은 1993년이다. 당시 SK는 대덕연구원 연구·개발(R&D) 조직 안에 신약개발연구팀을 만들었다. 처음부터 SK의 목표는 국내가 아닌 글로벌 시장이었다. SK는 국내 최초로 FDA의 임상시험 승인을 받기도 했다. 항우울제인 ‘YKP10A’가 주인공인데, 이 약은 2000년 글로벌 제약사인 얀센에 기술수출하기도 했다. 2007년 SK가 지주사로 전환하면서 신약개발사업부 이후 2011년 SK바이오팜으로 분사했다.
FDA로부터 임상시험 승인을 가장 많이 받은 국내 제약사도 SK바이오팜이다. SK바이오팜은 FDA로부터 총 16개의 임상시험 승인을 받았다. 업계 관계자는 “그동안 제약업계에서 ‘SK’하면 SK케미칼을 떠올렸으며, SK바이오팜은 존재감이 없었다”며 “가시적 성과가 없어도 25년간 끊임 없이 R&D에 투자했다는 것만으로도 의미는 충분하다”고 말했다.
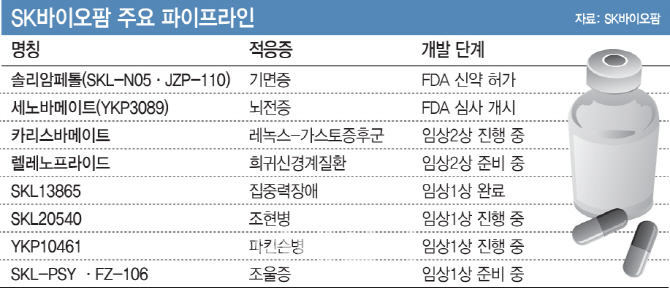
수노시에 이어 상용화 가능성이 높은 것은 뇌전증 치료제 ‘세노바메이트’다. 이 약은 임상3상을 마치고 지난해 말 FDA에 신약허가신청서를 제출해 놓은 상태로 이르면 올해 말 허가를 받아 2020년 상반기 미국에서 출시될 예정이다. 이외에도 희소질환인 레녹스-가스터증후군(소아뇌전증의 일종), 조현병, 파킨슨병, 조울증 치료제를 개발 중이다.
특히 세노바메이트는 국내 제약사가 독자적으로 개발해 FDA의 허가신청까지 마친 첫 신약이다. SK바이오팜 관계자는 “세노바메이트는 후보물질 도출부터 임상시험, 허가까지 기술이전이나 공동개발이 아닌 독자적으로 개발한다는 데 의의가 있다”며 “개발 실패 시 위험은 크지만 상용화에 성공하면 파트너사와 수익을 나누지 않기 때문에 부가가치가 크다”고 말했다.
SK바이오팜은 미국 내 판매도 직접 할 계획이다. 이를 위해 미국 현지에 SK라이프사이언스라는 법인을 운영 중이다. 후발주자에 현지 인지도가 전무해 결코 쉬운 일은 아니다. 이에 대해 또 다른 업계 관계자는 “기술이전을 하는 이유가 상용화까지 드는 막대한 비용과 실패가능성을 줄이려는 것”이라며 “개발부터 판매까지 독자적으로 한다는 것은 최고 의사결정자의 의지가 없다면 불가능하다”고 말했다.
최 회장은 제약·바이오산업을 제2의 반도체로 육성한다는 계획을 수차례 내비쳤다. 지난 2017년에는 의약품 위탁생산(CMO) 전문인 SK바이오텍이 아일랜드 BMS의 의약품 공장을, 지난해 7월에는 미국 의약품 위탁개발 및 생산(CDMO) 전문인 엠펙을 인수했다. 아시아, 유럽, 미국에 의약품 생산거점을 갖춘 것으로 세노바메이트는 허가 후 엠펙에서 생산할 것으로 예상된다.
|









![[포토] 폭설 피해](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900576t.jpg)
![[포토]최재해, '정치적 탄핵 매우 유감...자진 사퇴 생각 없다'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900431t.jpg)
![[포토]'모두발언하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112900370t.jpg)
![[포토]이데일리 퓨처스포럼 송년회 무대](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801622t.jpg)
![[포토]용산국제업무지구 개발계획 공동협약식에서 협약서 서명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801123t.jpg)
![[포토]이틀 연속 폭설에 눈 쌓인 북한산](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801096t.jpg)
![[포토]서울리빙디자인페어 in 마곡](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112800810t.jpg)
![[포토] 서울역 환승센터](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112800768t.jpg)
![[포토] 미국 캘리포니아 '석류' 첫 출시](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112800646t.jpg)
![[포토]'돈이 보이는 창' 찾은 함영진 우리은행 부동산리서치랩장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112801076t.jpg)


![[단독]SNS 성범죄 증거 삭제 막는다…'불법 영상물 보전명령 도입'](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24112900101b.jpg)

