|
항암백신 중 암 예방 백신은 기존 백신의 정의처럼 특정 장기를 감염시켜 암을 일으킬 수 있는 바이러스를 차단하는 약물이다. 하지만 대부분의 암은 바이러스나 세균 감염이 아닌 체내 유전자나 생활습관 등 복합적인 요인에 의해 발병한다. 단 하나의 물질을 차단해 병을 예방하기 어려운 셈이다. 이에 따라 암 치료 백신은 이미 암이 발생한 환자에서 재발 위험을 최소화하도록 암의 항원을 투입해 면역 시스템을 강화하는 백신으로 정의된다.
암 예방 백신은 미국 머크(MSD)의 ‘가다실’ 제품군과 영국 글락소스미스클라인(GSK)의 서바릭스 등 자궁경부암을 예방 목적의 약물 2종이 출시됐다. 반면 암 치료 백신의 경우 미국 덴드리온의 ‘프로벤지’가 전립선암 환자 대상으로 미국에서 2010년 최초로 승인됐지만, 약물의 세포 기반 생산 방식 등이 당시 의료체계와 맞지 않는 등의 이유로 인해 흥행에는 실패했다. 사실상 시장에서 인정받은 암 치료 백신은 아직 나오지 않은 셈이다.
정헌 애스톤사이언스 대표는 “암 치료 백신 시장은 성장 가능성이 크지만 뚜렷한 선두 주자가 없다”며 “기존 물질의 임상 뿐만아니라 새로운 물질의 추가 발굴에 힘써 회사의 가치를 높여 나가겠다”고 말했다.
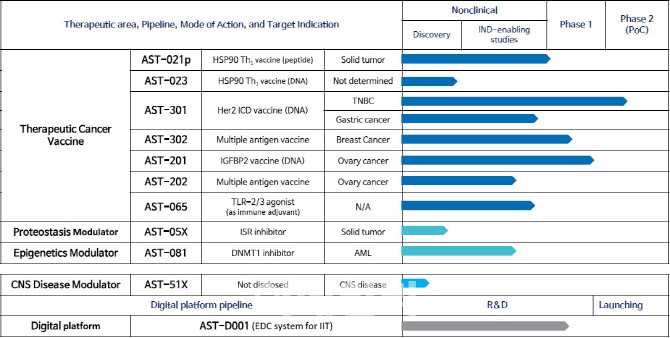
2018년에 설립된 애스톤사이언스는 현재 국내외 연구소로부터 도입한 암 치료 백신 후보물질 4종의 임상 개발을 진행 중이며, 3종의 추가물질에 대한 전임상 연구 및 신규물질 발굴 연구 등도 병행하고 있다. 이를 통해 회사는 2026년경 ‘임상 3상 이상’(2종)과 ‘임상 1/2상 이상’(8종) 등 총 10종의 유력한 암 치료 백신 후보물질을 확보하는 것을 염두에 두고 있다.
애스톤사이언스의 대표적인 후보물질은 AST-301과 AST-201, AST-302 등 3종이며, 2020년 이후 미국 워싱턴대 암백신연구소로부터 기술이전받은 것으로 확인됐다. 이들은 모두 T세포의 활성화를 돕는 항원의 유전자를 ‘플라스미드 디옥시리보핵산(DNA)’에 삽입해 체내로 전달하는 방식으로 설계된 것으로 알려졌다. AST301은 유방암이나 위암에서 나타는 HER2 항원을, AST-201과 AST-302는 각각 난소암에 있는 IGFBP2, 각종 고형암에서 나오는 HSP90라는 항원을 타깃한다.
|
애스톤사이언스의 주력 후보물질인 AST-301은 삼중음성유방암(미국, 호주, 대만 등 임상 2상 진행) 및 HER2 양성 위암(대만 임상 2상 진행) 등 2종의 적응증을 동시에 개발해 주목받고 있다. 해당 임상은 미국 머크(MSD)의 ‘키트루다’(성분명 펨브롤리주맙)이나 스위스 로슈의 ‘젤로다’(성분명 카페시타빈) 등과 같은 표준치료제와 AST-301을 병용 투여하는 방식으로 진행되고 있다.
이밖에도 애스톤사이언스의 AST201은 난소암 대상 미국 내 임상 2상을 준비 중이며, AST302은 유방암 대상 연구자 주도 임상 1상이 진행되고 있다. 회사는 지난해 6월에도 AST-202(다중항원 타깃)를 워싱턴대로부터 전임상 단계에서 기술이전 받기도 했다.
|
애스톤사이언스는 워싱턴대 이외에도 국내에서 고려대나 차백신연구소(261780)로 물질또는 관련 기술을 이전받아 개발 협력을 이어가고 있다.
먼저 회사는 지난 2019년 고려대로부터 펩타이드 물질 ‘AST-021p’을 기술이전 받았으며, 현재 표준치료법이 없는 재발성 혹은 진행성 고형암 대상 국내 임상 1상을 진행하고 있다. 또 애스톤사이언스는 차백신연구소로부터 총 2031억원 규모로 기술이전받은 면역증강제 ‘엘-팜포’(L-pampo)를 자사의 ‘AST-021p’나 ‘AST-023’ 등의 후보물질 등과 병용하는 전임상 연구도 병행하고 있다.
차백신연구소 관계자는 “엘-팜포는 ‘톨라이크수용체’(TLR) 2나 TLR3를 자극해 면역력을 높이는 효과가 있다고 분석된 물질이다”며 “암 치료 백신 후보의 효능을 엘-팜포가 증가시킬 수 있을 것을 기대하며, 연구가 진행중인 상황이다”고 설명했다.









![[포토]'규탄사하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120401162t.jpg)
![[포토]비상계엄 해제 후 한자리에 모인 한덕수 총리와 국무위원들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120401092t.jpg)
![[포토]최상목 경제부총리, '어두운 표정'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400960t.jpg)
![[포토]청사들어서는 한덕수 총리](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400786t.jpg)
![[포토] 대통령실 입구의 취재진](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400817t.jpg)
![[포토]'긴급 의원총회 참석하는 추경호 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400571t.jpg)
![[포토]'긴박했던 흔적들'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400485t.jpg)
![[포토]조국, '국가 비상사태 만든 이는 尹...탄핵해야'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400366t.jpg)
![[포토]尹, '비상 계엄 해제할 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400277t.jpg)
![[포토]코스피-코스닥 동반 상승 마감](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300908t.jpg)



![[속보]국무위원 전원, 한덕수 총리에 사의 표명](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24120401125h.jpg)
