[이데일리 왕해나 기자]
셀트리온(068270)이 개발한 코로나19 항체치료제 ‘렉키로나주’(성분명 레그단비맙, 코드명 CT-P59)의 허가 여부가 5일 결정된다.
식품의약품안전처는 이날 오전 10시 코로나19 치료제 최종점검위원회를 열고 셀트리온이 신청한 렉키로나주 조건부 허가 여부를 최종 결정한다. 회의 결과는 당일 공개할 방침이다.
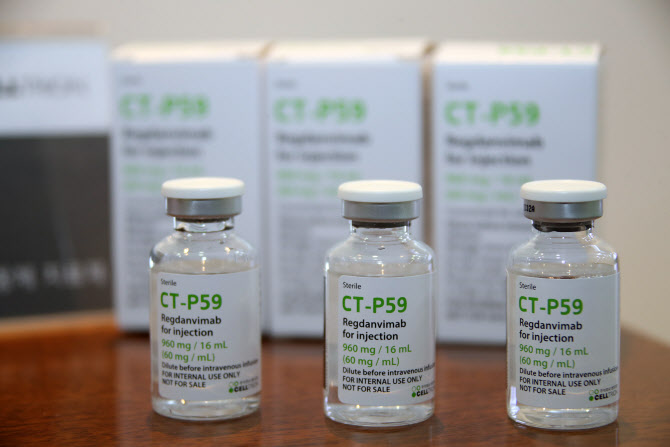 | | 셀트리온 코로나19 항체치료제 ‘렉키로나주’.(사진=연합뉴스) |
|
식약처는 코로나19 백신과 치료제를 허가하기 전 검증 자문단, 중앙약사심의위원회(중앙약심), 최종점검위원회로 이어지는 외부 전문가의 세 차례 조언 절차를 거치고 있다.
검증 자문단은 렉키로나주의 임상 3상 수행을 전제로 품목허가를 할 것을 권고했다. 자문단은 렉키로나주가 바이러스를 ‘양성’에서 ‘음성’으로 전환되는 시간에 대해서는 통계적 유의성을 확인하지 못했지만, 코로나19 증상 개선 시간을 3.43일 줄인 것으로 확인했다. 다만 입원이나 산소 치료가 필요한 환자 비율이 감소하는 경향(입원율)과 사망률에 대해서는 명확한 결론을 내리기 어렵다고 봤다.
중앙약심도 임상 3상 결과를 제출하는 것을 조건으로 허가할 것을 권고했다. 다만 렉키로나주를 고위험군 경증 환자와 중등증 환자에 한정해 투여해야 한다고 조건을 달았다. 경증 환자에게서는 통계적으로 유의한 수준의 치료 효과를 확인하지 못했다는 이유에서다.
이날 최종점검위원회는 앞서 진행된 치료제 안전성·효과성 검증 자문단과 이번 중앙약심 자문을 통해 얻은 전문가 의견, 효능·효과(안), 권고사항 등을 종합적으로 검토해 최종 결론을 내린다.
식약처 허가가 나면 셀트리온은 곧바로 치료제 공급에 착수할 예정이다. 이미 10만명에게 투약할 수 있는 제품 생산을 마친 상태다. 연내 렉키로나주 250만~300만명분을 추가로 생산할 계획이다.








![[포토]이가영,부드러운 티샷 공략](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100330t.jpg)
![[포토] '트릭 오어 트릿' 진행하는 바이든 대통령 부부](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103102211t.jpg)
![[포토] 송민혁 '이글 2개, 버디7개 잡은 날'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100152t.jpg)
![[포토]치솟던 배춧값 대폭 하락…"물량 충분해"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101370t.jpg)
![[포토]삼성전자 반도체 영업익 4조](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101369t.jpg)
![[포토]하모니카 연주가 이윤석의 연주](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101230t.jpg)
![[포토]민통선 주민들 트랙터 시위](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101122t.jpg)
![[포토] 서울시예산안 설명하는 오세훈 시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100890t.jpg)
![[포토] 벤틀리모터스코리아, '더 뉴 컨티넨탈 GT 스피드' 공개](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100418t.jpg)
![[포토] 2024 서울 문화원 엑스포](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103001770t.jpg)
![[포토]이가영,정상을 바라본다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100331t.jpg)



