박한오 바이오니아(064550) 회장은 최근 ‘SRN-001 임상 1상 진입 관련 주주님들께 드리는 글’을 통해 이같이 밝혔다. 박 회장이 직접 주주들과 소통에 나선 것은 이례적인 행보다. SRN-001의 임상 1상 진입이 바이오니아에 그만큼 의미가 깊다는 방증이다.
|
◇SRN-001, 연말까지 임상 1a상을 끝낼 예정
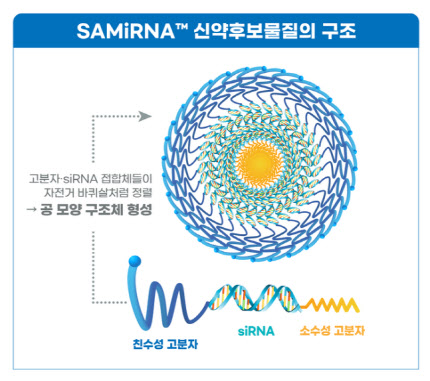
실제 SRN-001은 특발성 폐섬유증(IPF)을 적응증으로 하는 바이오니아의 핵심 파이프라인 중 하나다. 섬유화에 관여하는 성장인자인 ‘AREG 메시저리보핵산(mRNA)’를 높은 효율로 분해하는 siRNA에 기반한다. 바이오니아 자회사 써나젠테라퓨틱스의 물질특허 구조체인 SAMiRNA가 적용된 세계 첫 siRNA 신약후보물질이다.
SAMiRNA는 ‘초분자 siRNA 나노 구조체’라고도 하며 바이오니아가 원천특허를, 써나젠이 세계 독점실시권을 보유하고 있다. 양사는 이를 기반으로 한 신약후보물질들을 개발해 190여 건의 국내외 특허를 출원, 등록해 신약 파이프라인과 지식재산 포트폴리오를 강화해왔다.
이어 “이러한 문제점을 해결하고자 수많은 시도를 한 끝에, SAMiRNA라는 새로운 개념의 siRNA를 발명할 수 있었다”며 “SAMiRNA는 siRNA 치료제들의 고질적 부작용인 선천면역을 자극하지 않고, 혈관벽·세포막을 통과해 표적 조직·세포로 전달되는 효율이 우수하다”고 덧붙였다.
써나젠은 호주 임상시험기관 ‘CMAX’에서 연말까지 임상 1a상을 끝낼 예정이다. 이를 바탕한 결과보고서 등을 토대로 내년 미국 식품의약국(FDA)에 반복투여 임상 1상(1b) 및 환자를 대상으로 한 초기 임상 2상(2a)을 신청할 방침이다. 글로벌 시장조사업체 리서치앤마켓에 따르면 글로벌 IPF 치료제 시장은 연평균 7% 성장해 2030년 61억 달러(약 8조원) 규모로 커진다.
박 회장은 “인간을 대상으로 한 SRN-001의 임상에서 영장류 실험에서와 같은 결과가 검증된다면, SAMiRNA는 siRNA 신약개발의 새로운 지평을 열 것”이라며 “그동안 지속적으로 관심을 보인 글로벌 제약사들과의 협업 속도도 빨라지고, 바이오니아뿐만 아니라 인류의 난치병 치료를 위한 발전을 가속하는 트리거(기폭제)가 될 것”이라고 재차 강조했다.
◇“아무도 걸어가 보지 않았던 길 도전 과정서 시행착오”
SRN-001 임상 1상 진입으로 바이오니아의 충남 남공주산단 siRNA 의약품 제조 및 품질관리(GMP) 공장 건설도 속도가 날 것으로 기대된다. 박 회장은 siRNA GMP의 착공 시점도 구체적으로 제시했다.
예정보다 늦어졌지만 SRN-001 임상 1상 진입을 계기로 사업에 대한 강한 추진 의지를 내비친 셈이다. 바이오니아가 남공주산단 확보한 공장 부지는 6만여㎡다. 신소재 및 신약 공장 건설에 총 830억여원을 투입한다.
바이오니아의 siRNA GMP 공장 착공 목표는 2025년 현실화한다고 해도 당초 수립했던 계획보다 지연되는 것이다. 앞서 바이오니아는 2021년 충남도와 남공주산단 공장용지 투자협약을 맺고, siRNA GMP 공장 건설에 들어갈 것을 약속한 바 있다.
박 회장은 “아무도 걸어가 보지 않았던 길에 도전하는 과정에서 많은 시행착오를 겪었다”며 “그동안 축적된 바이오니아의유전자 기술력을 통해 세계 인류의 건강과 삶의 질 향상에 기여하는 글로벌 헬스케어 기업으로 도약하는 데 모든 노력을 다해 나가겠다”고 역설했다.
|









![[포토] 오세훈 서울시장, '리더는 세상을 어떻게 바꾸는가'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700981t.jpg)
![[포토]서울에 117년만에 폭설](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700882t.jpg)
![[포토] 휘슬러x구세군 사랑샘 자선냄비 체험관 전달식](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700766t.jpg)
![[포토]격차해소특별위원회 정책토론회 '정년연장 쟁점과 과제'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700657t.jpg)
![[포토]박찬대, '군주민수'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700587t.jpg)
![[포토]발렌타인 글렌버기 스몰배치 16년 출시](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700578t.jpg)
![[포토] '금융권 공감의 장' 인사말하는 이병래 회장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600936t.jpg)
![[포토]경북 국립의대 신설 촉구, '참석자들에게 인사하는 한동훈'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600846t.jpg)
![[포토]손태승 전 회장, 영장실질심사 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600794t.jpg)
![[포토]정윤하 등장](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600056t.jpg)




