24일 미국 국립보건원(NIH) 임상시험정보사이트 ‘클리니컬 트라이얼즈’ 등에 따르면 CG인바이츠는 이달 중순 아이발티노스타트 2a상 환자 모집에 들어갔으며, 지난주 첫 환자 투여까지 이뤄졌다.
|
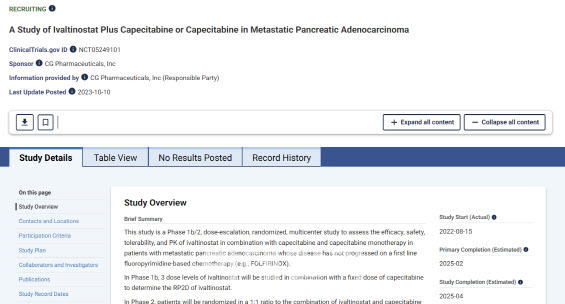
이번 2a상은 진행성 또는 전이성 췌장암 환자 중 폴피리녹스 요법 후 질병이 진행되지 않은 환자 총 52명을 대상으로 실시된다. 환자는 아이발티노스타트와 카페시타빈(capecitabine)을 병용 투여하는 시험군과 카페시타빈 단독 요법의 대조군으로 나눠진다. 1차 평가변수는 무진행생존기간(PFS)이며 이어 질병통제율(DCR), 전체생존기간(OS) 등의 유효성을 비교한다.
4제 복합제인 폴피리녹스(옥살리플라틴, 이리노테칸, 플루오로우라실, 류코보린)는 전이성 췌장암에서 타 요법에 비해 치료효과가 우수하다. 그러나 독성 등의 부작용 위험과 짧은 생존 기간으로 오랜 기간 투여하기 어렵다. 따라서 이후에도 사용할 수 있는 치료제가 필수적임에도 마땅한 치료제가 없는 상황이다. 이에 CG인바이츠가 아이발티노스타트 유지요법 임상에 나선 것이다.
환자 스크리닝으로 성공 가능성 높여
CG인바이츠는 2a상 피험자를 1차 치료제에서 반응을 보인 환자로 한정해 더 좋은 데이터를 얻을 것으로 기대 중이다.
CG인바이츠는 환자 스크리닝으로 인해 임상이 지연되는 것을 막고 더 빠르게 환자를 모집하기 위해 임상 사이트도 늘렸다. 기존 1b상에서는 8개의 의료기관에서 환자를 모집했지만 2a상은 총 13곳에서 환자 모집 및 투약이 이뤄진다.
임상 사이트를 확대해 환자 모집에 대한 부담을 줄인 만큼 속도감 있는 임상이 기대된다. 2a상은 아이발티노스타트 2주 투여 후 1주 휴식 등 3주 사이클로 이뤄지며, 총 10차례 반복된다. 환자별로 투약에 30주의 시간이 소요되는 셈이다.
CG인바이츠 관계자는 “환자 개인에 약 8개월 동안 투약이 이뤄지는데 1b상 이후 환자들의 대기가 이미 많다”라며 “최대한 빠르게 환자 등록을 끝내 내년 11월까지는 모든 투약을 마칠 것”이라고 설명했다.
내년말 기술수출 기대…췌장암 대상 유일 HDAC 억제제
CG인바이츠는 HDAC 억제제 계열의 아이발티노스타트가 여러 측면에서 가치가 높다고 판단하고 있으며, 이에 2a상을 거쳐 효과 확인 후 기술수출할 것으로 예상된다.
전세계적으로 HDAC 저해제는 약 250건이 개발 중인데 이 중 약 140건이 혈액암(약 53%), 고형암 90건(약 35%)이다. 이밖에 유방암, 폐암, 신세포암, 난소암 등 다양한 암 종을 적응증으로 개발되고 있는데 췌장암 적응증으로는 아이발티노스타트가 유일하다.
현재 미국 식품의약국(FDA)로부터 승인된 HDAC 저해제 약물은 머크 ‘졸린자’(피부 T-세포림프종), 셀진 ‘이스토닥스’(피부 T-세포림프종/말초 T-세포림프종), 온세오 ‘벨레오닥’(말초 T-세포림프종), 노바티스 ‘파리닥’(다발성골수종) 모두 혈액암으로만 허가된 상황이다.
특히 최근 종근당이 노바티스에 1조7000억원 규모로 기술수출한 물질이 이와 같은 HDAC 억제제 계열로 알려지면서 아이발티노스타트 기술수출 기대감은 더 높아질 것으로 보인다.
또 글로벌 시장조사기관 GBI리서치에 따르면 2021년 전 세계 췌장암 치료제 시장 규모는 약 3조3500억원에 달한다. 이어 2026년에는 약 5조5000억원까지 성장할 것으로 집계되면서 아이발티노스타드의 가치도 상당할 것으로 기대된다.
CG인바이츠 관계자는 “임상 2a상까지 성공적으로 수행한 뒤 기술수출했을 때 계약 규모가 몇배는 더 커질 수 있다”라며 “성공적인 임상을 위해 더 노력할 것”이라고 말했다.








![[포토] 오세훈 서울시장, '리더는 세상을 어떻게 바꾸는가'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700981t.jpg)
![[포토]서울에 117년만에 폭설](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700882t.jpg)
![[포토] 휘슬러x구세군 사랑샘 자선냄비 체험관 전달식](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700766t.jpg)
![[포토]격차해소특별위원회 정책토론회 '정년연장 쟁점과 과제'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700657t.jpg)
![[포토]박찬대, '군주민수'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700587t.jpg)
![[포토]발렌타인 글렌버기 스몰배치 16년 출시](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700578t.jpg)
![[포토] '금융권 공감의 장' 인사말하는 이병래 회장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600936t.jpg)
![[포토]경북 국립의대 신설 촉구, '참석자들에게 인사하는 한동훈'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600846t.jpg)
![[포토]손태승 전 회장, 영장실질심사 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600794t.jpg)
![[포토]정윤하 등장](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600056t.jpg)




