|
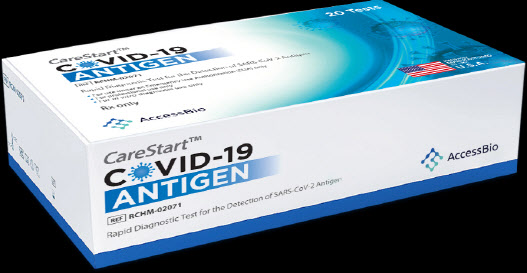
4일 FDA 긴급사용승인 허가를 받은 제품은 `CareStartTM COVID-19 Antigen Home Test`로, 이번 승인을 통해 엑세스바이오 제품은 처방전 없이도 온라인 또는 오프라인으로 어디서든 구매가 가능해진다.
엑세스바이오 측 관계자는 “미국 질병통제예방센터(CDC)에 따르면 현재 미국 인구의 49.7%가 백신 접종을 완료했지만, 다른 나라에 비해 백신 접종 속도가 빠름에도 불구하고 델타 등 다양한 변이로 인해 확진자 수가 빠르게 다시 증가하고 있다”며 “이는 감염 확산 방지를 위해 여전히 코로나19 진단이 중요하다고 해석할 수 있는 만큼 처방전 없이 손쉽게 구매할 수 있는 코로나 자가진단키트의 유용성 또한 높을 것으로 기대된다“고 말했다.
미 FDA의 긴급사용승인 허가를 받은 OTC(Over-the-Counter, 처방전 없이 구매 가능 제품) 진단제품은 오라슈어(OraSure Technologies, Inc.)와 애보트(Abbott laboratories), 퀴델(Quidel Corporation) 및 엘룸(Ellume Limited)에 이어 엑세스바이오가 다섯 번째다. 이 제품은 긴급사용승인 허가를 위해 진행한 임상실험에서 민감도는 87%, 특이도는 98%을 나타내며 글로벌 기업에 대등하는 우수한 성능을 입증했다.







![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]영화 속 배경에서 찰칵](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901369t.jpg)
![[포토] 아수라장된 기자회견장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901115t.jpg)
![[포토]다양한 식음료가 한 자리에, '컬리 푸드페스타 2024'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900958t.jpg)
![[포토]2025학년도 정시 대학입학정보박람회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900743t.jpg)
![[포토]북적이는 정시 대학입학정보박람회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900708t.jpg)
![[포토] 미소짓는 오세훈 서울시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900574t.jpg)

![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)


![[속보]민주당, 韓대행 특검법 공포 시한 24일로 결정](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24122200149h.jpg)