|
[이데일리 김지섭 기자] 과학기술의 눈부신 발전은 인류의 삶을 보다 풍요롭고 편리하게 만듭니다. 특히 ‘바이오의약품’은 그동안 고칠 수 없던 병을 치료하고 건강한 삶을 누릴 수 있도록 돕고 인류가 갖고 있는 ‘생명연장의 꿈’을 현실로 만들고 있습니다.
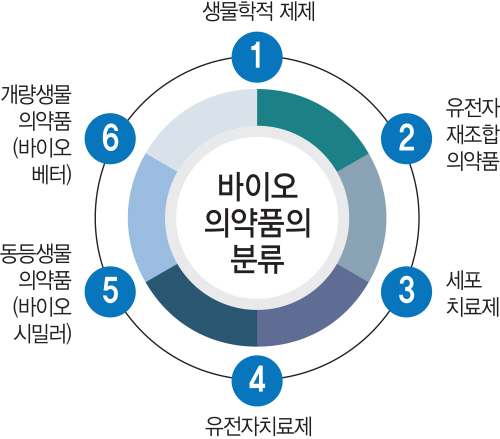
바이오의약품은 사람이나 다른 생물에 있는 단백질·유전자·세포 등을 원료로 만든 의약품입니다. 화학물질을 인공적으로 합성해 만든 ‘합성의약품’과는 달리, 문자 그대로 생명·생물이라는 의미의 ‘바이오’에 뿌리를 둔 의약품입니다. 사람이나 동물에서 치료 능력이 있는 세포로 만드는 ‘세포치료제’와 몸 속에 흐르는 피에서 유용한 물질을 가져다 만드는 ‘혈액제제’, 약해졌거나 죽은 세균 및 바이러스를 몸 속에 넣어 몸 속의 면역기능을 높이는 ‘백신’, 개인마다 갖고 있는 유전물질을 몸 속에 넣거나 교정해 만드는 ‘유전자치료제’ 등이 모두 바이오의약품입니다.
인공적으로 만들어진 합성의약품은 기본적으로 몸에서 거부반응을 일으키기 쉽습니다. 하지만 바이오의약품은 보다 안전하면서 효과가 뛰어난 것이 특징입니다. 전 세계적으로 제약사들이 바이오의약품 개발에 집중하는 이유입니다. 이미 글로벌 신약개발 흐름은 바이오의약품으로 이동하고 있습니다. 세계 최대 의약품시장인 미국을 보면 이 같은 흐름이 더욱 분명합니다. 미국 식품의약국(FDA)은 지난 2008년부터 지난해까지 총 321건의 신약을 허가했습니다. 이중 71건이 바이오신약입니다. 바이오신약 승인 비중은 2008년 14.3%에서 지난해 35.3%로 늘어났습니다. 앞서 설명한대로 바이오의약품은 합성의약품보다 부작용이 적기 때문에 신약을 개발하는 과정에서 성공할 확률도 합성의약품(6.2%)보다 바이오의약품(11.5%)이 높습니다. 앞으로 효능이 뛰어난 바이오의약품은 더욱 쏟아져나올 것으로 보입니다.
시장에서 차지하는 비중도 점점 커지고 있습니다. 의약품 시장조사기관 아이큐비아에 따르면 2016년 기준 세계 의약품 시장 규모는 1조 1050억달러였습니다. 이중 바이오의약품 비중은 2220억달러로 19.9%를 차지했습니다. 바이오의약품 시장 규모는 앞으로 5년 동안 연평균 9.4%로 가파르게 성장하면서 2021년에는 전 세계 의약품 시장에서 23.4%에 해당하는 3440억달러까지 클 전망입니다.
글로벌 제약매체 피어스파마가 집계한 2016년 기준 세계에서 가장 많이 팔린 의약품 10개 중 8개가 바이오의약품이었습니다. 전 세계에서 가장 잘팔리는 약은 애브비의 ‘휴미라’로 160억 8000만달러 어치가 팔렸습니다. 이어 암젠의 ‘엔브렐’은 88억 7000만달러, 로슈의 ‘리툭산’은 85억 8000만달러의 매출을 올렸습니다. 이처럼 바이오의약품은 개발 규모나 매출 면에서도 기존 합성의약품을 넘어서면서 인류 건강의 핵심 요소로 자리를 잡고 있습니다.
바이오의약품은 생명공학 발전에 따라 진화를 거듭해왔습니다. 1909년 독일 면역학자 에를리히가 매독균에만 선택적으로 작용하는 화학물질을 배양하면서 매독치료제를 개발한 것이 시초입니다. 1973년에는 미국 과학자 스탠리 코헨과 허버트 보이어 박사가 인간의 유전정보가 담겨 있는 ‘DNA’를 시험관 안에서 다른 생물체의 DNA와 결합해 새로운 유전정보를 갖는 생물체를 만들어 내면서 생명공학 연구의 새로운 지평을 열었습니다. 이후 1980년대에 생물체의 DNA를 시험관에서 증폭할 수 있는 기술을 개발하면서 유전자재조합 기술이 널리 쓰이기 시작했습니다.
이 기술을 활용해 만든 것이 ‘인간 인슐린’을 생산하는 대장균입니다. 인슐린은 사람 몸 속에서 혈당을 조절하는 중요한 호르몬으로 췌장에서 만들어집니다. 일부 사람들은 인슐린을 생산하지 못해 돼지나 소에서 추출한 인슐린을 사용했지만, 몸속에서 거부반응을 일으켜 사망하기도 했습니다. 그러나 미국 일라이릴리가 하룻밤에 몇백만개로 증식하는 대장균을 통해 인간 인슐린을 배양, 1982년 이를 상품화한 ‘휴물린’을 허가받습니다. 이후 성장호르몬 ‘프로트로핀’(1985년), 항바이러스성 단백질 인터페론인 ‘인트로에이’(1986년), 빈혈치료제 ‘에포젠’(1989년) 등 단백질을 재조합한 1세대 바이오의약품이 쏟아져 나왔습니다.
|
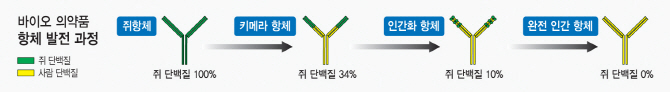
2세대 바이오의약품은 항체의약품입니다. 세균이나 바이러스 등 외부물질인 ‘항원’이 침투할 경우 이와 맞서 싸우기 위해 혈액이 만드는 단백질인 ‘항체’ 반응을 이용해 만듭니다. 처음에는 쥐에서 유래한 항체를 사용했지만 사람 몸에 맞지 않아 부작용이 생겼습니다. 이후 쥐에서 나온 항체와 사람 몸에서 나온 항체를 결합한 ‘키메라 항체’, 온전히 사람 유래로 만든 ‘사람 항체’ 등 기술이 발달하면서 다양한 항체의약품이 나왔습니다. 휴미라·엔브렐 등이 모두 항체의약품입니다.
그러나 항체의약품은 세포를 배양하고 정제하는 것이 쉽지 않아 다국적 제약사들의 전유물로 인식됐습니다. 또 1세대 바이오의약품은 분자 구조가 단순해 낮은 비용으로도 비교적 쉽게 제품 개발이 가능했지만, 2세대 바이오의약품은 분자 구조가 복잡해 개발이 어렵고 막대한 글로벌 임상비용으로 진입 장벽이 높았습니다. 특히 복잡한 항체의약품을 복제하는 것은 불가능에 가깝다는 의견도 지배적이었습니다.
3세대 바이오의약품은 사람 세포를 추출한 뒤 배양·조작해 다시 이식하는 ‘세포치료제’, 유전자 조작 기술을 활용해 유전자 결함을 제거하거나 치료 기능을 넣는 ‘유전자치료제’ 등이 있습니다. 지금까지 치료가 어려웠던 난치병 등을 고치기 위해 많은 제약사들이 3세대 바이오의약품 개발에 뛰어들고 있습니다. 우리나라에서는 파미셀, GC녹십자셀, JW크레아젠 등이 3세대 바이오의약품을 개발하고 있습니다.
◇‘바이오혁신’이 가져올 ‘바이오경제’ 시대 눈앞
지난 2009년 경제협력개발기구(OECD)는 이처럼 바이오기술이 발전하고 정보기술(IT), 나노기술(NT) 등 첨단 신기술과 융합하면서 오는 2030년 ‘바이오경제’ 시대가 올 것으로 내다봤습니다. 바이오경제는 바이오기술을 통해 인류의 복지와 경제성장을 동시에 달성하는 새로운 패러다임을 의미합니다. 과학기술정보통신부에 따르면 글로벌 바이오시장은 반도체·자동차·화학제품 등 3대 산업의 합계를 넘어 2015년 1조 6000억달러에서 2030년 4조 4000억달러까지 성장할 전망입니다. 이에 미국·유럽·일본 등 선진국은 바이오의약품을 미래 성장동력으로 확보하고 기술 선점을 위해 정부 차원에서 육성 전략을 앞다퉈 수립하고 있습니다. 우리나라도 과기정통부를 주축으로 교육부, 농식품부, 산업부 등 8개 부처의 의견을 수렴해 ‘바이오경제 혁신전략 2025’를 수립, 추진하고 있습니다. 과기정통부는 지난 2016년까지 진행한 제2차 기본계획에서 확보된 투자 성과를 바탕으로 신기술·신산업을 키우고 글로벌 진출을 본격화해 바이오경제 시대를 주도하는 바이오강국을 실현한다는 포부입니다.
|








![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]영화 속 배경에서 찰칵](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901369t.jpg)
![[포토] 아수라장된 기자회견장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901115t.jpg)
![[포토]다양한 식음료가 한 자리에, '컬리 푸드페스타 2024'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900958t.jpg)

![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)