8일 퓨쳐켐에 따르면 FC705의 국내 및 미국 임상이 순항하고 있으며, 1상 결과를 바탕으로 올해 결과 발표 및 기술수출 계약 체결 등이 기대되는 상황이다. FC705는 전립선 암에 과발현되는 단백질 ‘PSMA’(Prostate Cancer Membrane Antigen)를 표적하는 화합물에 치료용 동위원소 ‘177-루테튬’을 도입한 치료제다.
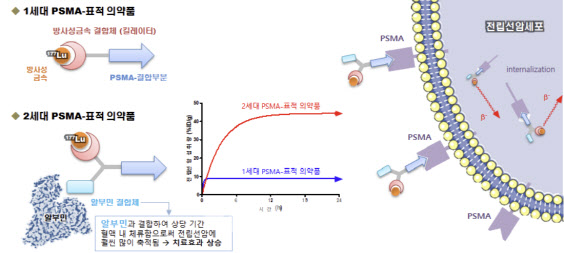
구체적으로, 반감기가 7일 미만인 방사성 동위원소 ‘177-루테튬’을 분자의약품 PSMA에 부착하는 방식이다. 해당 물질은 전립선암에 축적돼 항암 효과를 나타내며, 전립선 암세포가 다량으로 발생한 항원에 결합하기 때문에 건강한 세포에 대한 손상은 최소화할 수 있는 것으로 알려졌다.
또 FC705는 알부민 결합체가 도입된 2세대 의약품에 속하며 다른 화합물에 비해 친수성이 높아 비특이적결합이 기본적으로 낮은 특성을 가진다.
|
전립선암 대상 현재 미국 FDA로부터 허가받은 방사성 의약품은 노바티스의 ‘플루빅토’ (PSMA-617)가 있다. FC705의 직접적 경쟁 제품인 셈인데, FC705는 플루빅토 대비 적은 용량으로도 더 좋은 효과를 보여 부작용 이슈에서도 비교적 자유롭다는 장점이 있다.
전립선암 진단 방사성의약품 ‘FC303’과의 시너지도 기대된다. FC303은 PSMA 단백질을 표적으로 하는 진단 약물로 진단과 치료에 대한 토탈케어가 가능해지는 셈이다.
퓨쳐켐 관계자는 “FC303과 FC705는 동위원소 부분만 다르고 모두 PSMA를 타깃으로 하기 때문에 진단과 치료 모두에서 효과적으로 활용이 가능하다”고 설명했다.
올해 FC705 성과 가시화…10월 내 기술수출 본계약 결론
특히, 퓨쳐켐은 올해 남은 기간 동안 FC705 개발과 임상에 대한 결과와 성과를 수확할 예정이다.
퓨쳐켐은 올해 4월 중국 HTA와 전립선암 치료용 방사성의약품 FC705의 공동개발 및 독점 판권 관련 합의를 담은 텀 싯(Term Sheet) 계약을 체결한 바 있다. 양사는 실사 등의 과정을 마무리하고 본계약을 텀 싯 계약 체결 6개월 내인 올해 10월 안으로 체결하기로 예정돼 있다.
퓨쳐켐은 텀 싯 계약을 바탕으로, 본계약을 체결한다면 선급금(Upfront fee) 900만달러(약 120억원)에 순 매출액에 따른 별도의 로열티(Royalty)로 15년간 최대 18%를 취득할 것으로 예상된다. 특히, 중국 내 임상 개시가 빠르게 이뤄지면 1년 내 수령할 수 있는 금액은 250억원 가량이 될 것으로 추정된다.
이어 오는 10월에는 유럽종양학회(ESMO)에서 미국 임상 1상 결과를 발표한다. 퓨쳐켐에 따르면, 임상 결과 단회 투여를 진행한 6명의 환자 중 8주차까지 5명의 환자에서 ORR(객관적 반응률)과 DCR(질병통제율)은 100%로 나타났다. 또 임상에 참여한 모든 환자에게서 PSA(전립선 특이항원) 감소가 확인됐다.
퓨쳐켐 관계자는 “4월에 텀 싯 계약을 체결했고 당시 6개월 내로 본계약 체결 여부를 결정하기로 했기 때문에 10월내로 결과가 나올 예정”이라고 말했다.













![[포토]박성재 법무장관·조지호 경찰청장 탄핵안 가결...즉시 직무 정지](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121201103t.jpg)
![[포토] 작품이 된 생활용품](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200968t.jpg)
![[포토]조국, 징역 2년 확정..의원직 상실](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200952t.jpg)
![[포토] 롯데뮤지엄, '뷔르템베르크 왕실의 주얼리 세트' 전시](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200856t.jpg)
![[포토]법정 나서는 조국혁신당 의원들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200841t.jpg)
![[포토]야6당, '12.3 내란 사태' 국정조사 요구서 제출](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200820t.jpg)
![[포토]이재명 대표 만난 정순택 대주교](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200816t.jpg)
![[포토]국민의힘 새 원내대표에 ‘친윤’ 중진 권성동 의원 선출](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200800t.jpg)
![[포토]與 ‘탄핵 가결’ 급물살… 한동훈도 ‘찬성’ 돌아섰다](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200673t.jpg)
![[포토]발표하는 김동헌 고려대 경제학과 교수](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121200511t.jpg)

![[포토]박현경,자기 관리 중요해요](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121100160h.jpg)


