|
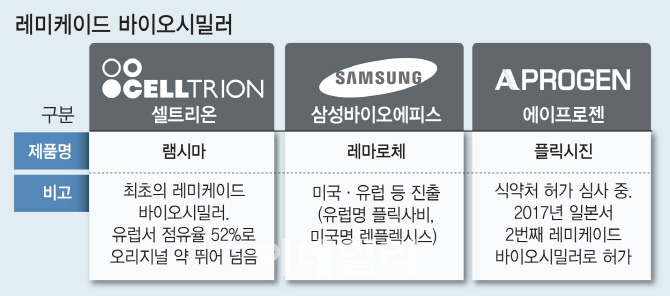
24일 업계에 따르면 국내 바이오벤처 에이프로젠은 지난달 ‘플릭시진’의 시판 허가를 식품의약품안전처에 신청했다. 플릭시진이 허가를 받을 경우 램시마와 삼성바이오에피스 ‘레마로체’(유럽명 플릭사비·미국명 렌플렉시스)에 이어 국내 세 번째 레미케이드 바이오시밀러가 된다.
레미케이드는 글로벌 제약사인 얀센의 의약품으로 류머티스관절염과 건선, 건선성 관절염, 강직성 척추염, 성인궤양성대장염, 소아 및 성인 크론병 등에 쓴다. 이 약은 자가면역질환 자체를 없앨 수는 없지만 면역계의 이상 작동을 누그러뜨려 증상이 생기지 않게 조절한다. 레미케이드는 지난해 전 세계에서 77억 8400만달러(약 8조 4000억원)의 매출을 올리며 의약품 순위 5위에 이름을 올렸다.
에이프로젠이 개발한 플릭시진은 이미 일본시장에서는 램시마에 이어 두 번째로 레미케이드 바이오시밀러가 됐다. 이 약은 2015년 일본에서 임상3상을 마무리하고 지난해 일본 니치이코제약을 통해 현지에서 품목허가를 받았다. 에이프로젠 관계자는 “레미케이드 바이오시밀러 중 유일하게 일본에서 임상시험을 진행했다”며 “미국 진출은 2016년 시작한 임상3상을 마무리하는 대로 미국 식품의약국(FDA)에 품목허가를 신청할 것”이라고 말했다. 유럽시장은 터키부터 공략할 예정이다.
램시마가 앞장서고 플릭사비(레마로체)가 뒤를 쫓는 유럽 레미케이드 바이오시밀러 시장에는 또 다른 경쟁자가 나타났다. 글로벌 제약사 노바티스의 바이오시밀러 전문 자회사인 산도즈가 올해 2분기 유럽의약품청으로부터 ‘제슬리’ 판매 허가를 받았기 때문이다. 이로써 유럽에서는 오리지널인 레미케이드와 세 개의 바이오시밀러가 경쟁을 펼치게 됐다.
유럽시장은 램시마가 오리지널을 제치고 ‘퍼스트 바이오시밀러’ 효과를 톡톡히 누리는 상황. 램시마는 지난해 4분기 유럽 시장 점유율 52%를 기록하며 레미케이드를 제쳤다. 업계에서는 올해에는 이 격차가 더 벌어질 것으로 예상하고 있다. 셀트리온 관계자는 “제슬리가 출시되면 유럽에서 분명히 경쟁은 더 심해질 것”이라며 “하지만 램시마의 브랜드 파워와 임상데이터가 견고하기 때문에 후발주자가 램시마의 아성을 쉽게 따라오지는 못할 것”이라고 말했다.
국내 약가제도도 바이오시밀러의 성장을 더디게 하는 원인으로 꼽힌다. 바이오시밀러나 제네릭(화학적 의약품 복제약) 같은 복제약은 통상적으로 오리지널 약 가격의 70% 선에서 출시한다. 그런데 우리나라는 복제약이 허가를 받으면 오리지널 약의 가격도 30% 정도 떨어진다. 사실상 복제약의 가격경쟁이 무의미한 상황에 놓이는 것.
긍정적인 것은 국내에서 전년 동기대비 매출 증가폭은 레미케이드가 12.8%에 불과한 반면 램시마는 29.8%로 꾸준히 격차를 좁히고 있다. 레마로체의 경우 지난해 1분기에는 매출이 전혀 없었지만 올해 1분기에는 미약하지만 매출이 발생했다. 한 업계 관계자는 “국내에서는 램시마와 레마로체가 지속적으로 매출을 늘리고 있고 플릭시진까지 시장에 등장하면 바이오시밀러에 대한 인식이 달라질 것”이라며 “해외에서는 국산 바이오시밀러들의 경쟁이 더 치열하게 펼쳐질 것으로 본다”고 말했다.








![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]영화 속 배경에서 찰칵](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901369t.jpg)
![[포토] 아수라장된 기자회견장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121901115t.jpg)
![[포토]다양한 식음료가 한 자리에, '컬리 푸드페스타 2024'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121900958t.jpg)

![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)