24일 제약·바이오업계에 따르면 GC녹십자의 미국 자회사 큐레보(Curevo)는 지난해 10월 대상포진 예방 백신 후보물질 ‘CRV-101’의 미국 임상 2b상 환자 투약을 마치고 3월 이내 톱라인 결과를 발표할 예정이다. 최종 임상완료 목표시점은 2028년 9월이다.
|
‘프리미엄 백신 사업’ 성공의 가늠자
‘수두-대상포진 바이러스’에 의해 발생하는 대상포진은 과거에 수두에 걸린 적 있거나 생백신(병원체를 인위적으로 약화시켜 직접 사용)인 수두 백신의 특성상 수두 예방접종을 한 사람에게서 발병한다. 대상포진 예방 백신은 이미 상용화된 제품만 세 개인데다 국내외 기업 여럿이 신규 백신 개발을 위해 임상을 진행 중일 정도로 시장 경쟁이 치열하다. 녹십자는 CRV-101을 시작으로 글로벌 프리미엄 백신 시장을 공략하겠다는 목표다.
녹십자가 2018년 미국에 자회사 큐레보를 설립한 것은 차세대 먹거리인 프리미엄 백신의 개발 및 상용화를 용이하게 진행하기 위해서다. 프리미엄 백신은 기초 백신보다 가격이 높고 성인 위주로 접종되며 미국과 유럽을 중심으로 시장이 형성돼 있다. 이제까지 독감, 수두, B형 간염 등 기초 백신에 집중해 온 녹십자에 CRV-101는 첫 프리미엄 백신 개발 과제라는 점에서 의미가 있다. 대상포진 예방 백신은 폐렴구균, 자궁경부암, 로타바이러스를 비롯해 대표적인 프리미엄 백신 중 하나로 꼽힌다. CRV-101이 성공해야 녹십자 프리미엄 백신 사업에도 힘이 실릴 수 있다는 분석이다.
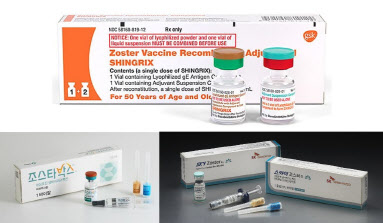
다만 주목해야 할 것은 싱그릭스의 무서운 성장세다. 현재 상용화된 대상포진 백신은 △미국 머크(MSD)의 ‘조스타박스’(2006년 FDA 허가) △영국 GSK의 ‘싱그릭스’(2017년 FDA 허가) △SK바이오사이언스 ‘스카이조스터’(2017년 식약처 허가) 총 3종이다. 싱그릭스는 후발주자이고 두 번의 접종이 필요하다는 단점에도 이제까지 출시된 대상포진 예방 백신 중 가장 예방효과가 높아 글로벌 점유율 90%를 차지하며 시장을 재편했다.
|
“후발주자 ‘싱그릭스’ 성공했듯이”…우월성 입증이 관건
녹십자는 조스타박스보다 10년 이상 늦게 출시된 싱그릭스가 시장을 주도하고 있다는 점을 들어 CRV-101도 싱그릭스 대비 우월성만 입증할 수 있다면 충분히 글로벌 대상포진 백신 시장에서 유의미한 성적을 거둘 수 있을 것으로 본다. 녹십자는 CRV-101의 예방효과를 싱그릭스와 유사한 수준으로 가져가면서도 면역증강제 투여량을 낮춰 안전성을 높여 경쟁력을 확보하겠다는 전략이다.
녹십자 관계자는 “싱그릭스와 직접 비교한 것은 아니지만 1상에서 CRV-101는 3등급 이상의 중증 부작용이 나타나지 않았고 주사 부위 통증을 포함한 2등급 부작용도 전체 시험군의 6.5% 이하에서만 발생했다”며 “싱그릭스가 시장을 재편했듯 경쟁력만 있다면 시장점유율을 뺏어올 수 있을 것”이라고 기대감을 드러냈다. 싱그릭스의 경우 접종 7일 이내 보고된 주사부위 및 전신 이상반응이 빈번했고 3등급 이상 이상반응도 17% 수준이었다. 3등급 이상의 부작용은 일상생활을 하지 못하는 수준의 반응을 의미한다.
문제는 현재 개발 중인 대부분의 대상포진 예방 백신들이 ‘싱그릭스 동등 이상의 효과’를 주장한다는 점이다. 현재 대상포진 예방 백신 ‘EG-HZ’의 임상 2상을 준비 중인 아이진 역시 호주에서 싱그릭스와 효능을 비교하는 임상 1상을 진행, 효능이 유사하다는 결과를 받았다. 이 때문에 녹십자는 임상 2b상에서 싱그릭스 대비 확실한 우월성을 보여줘야 향후 시장성을 기대해 볼 수 있다.
임상 2b상은 50세 이상 678명을 세 A, B, C 세 군으로 나눠 각각 CRV-101 저용량과 고용량, 싱그릭스를 투약해 비교하는 방식으로 이뤄지고 있다. 주요 지표는 △접종 7일 이내 국소 및 전신 반응 △29일 이내 이상반응 및 이상반응의 심각도, 예방접종과의 관련성 △심각한 이상반응 발생 빈도 △3개월 이내 백신 접종으로 인한 백신 단백질 특이적 항체 농도(GMC) 등이다.









![[포토]'이제 겨울'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112700287t.jpg)
![[포토] '금융권 공감의 장' 인사말하는 이병래 회장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600936t.jpg)
![[포토]경북 국립의대 신설 촉구, '참석자들에게 인사하는 한동훈'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600846t.jpg)
![[포토]손태승 전 회장, 영장실질심사 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600794t.jpg)
![[포토]정윤하 등장](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600056t.jpg)
![[포토]내년에 또보자 가을](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600715t.jpg)
![[포토]민주당 민생연석회의 참석하는 이재명 대표](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600655t.jpg)
![[포토] '소상공인 힘보탬 프로젝트' 발표](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600583t.jpg)
![[포토]정부, 국무회의에서 세번째 `김여사 특검법` 거부권 건의 의결](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112600579t.jpg)
![[포토] 이즈나 데뷔](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24112500181t.jpg)




