16일 식품의약품안전청에 따르면 지난해 총 690건의 의약품 임상시험 계획이 식약청의 승인을 받았다. 작년에 제약업체, 연구기관들이 신약이나 개량신약을 개발하거나 기존 제품의 새로운 효능을 검증하기 위한 연구를 총 690건 착수했다는 의미다.
이는 2011년 503건보다 37.2% 늘어났고 2010년 439건보다 57.2% 증가한 수치다. 제약업체들의 신약개발 활동이 활발해졌을 뿐만 아니라 국내 임상기관의 수준이 향상돼 다국적제약사의 임상 참여도 늘고 있다는 분석이다.
|
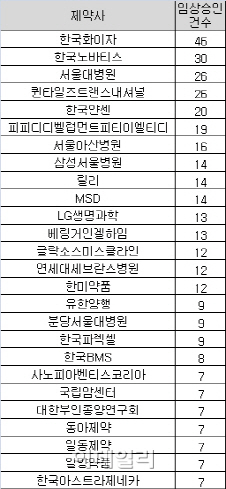
서울대학교병원(26건), 서울아산병원(16건), 삼성서울병원(16건) 등 주요 병원들도 연구 목적의 임상시험에 적극적으로 참여했다.
국내제약사 중에는 LG생명과학이 가장 많은 13건의 임상시험에 돌입했다. LG생명과학은 지난해 허가받은 당뇨병 치료신약 ‘제미글로’에 또 다른 당뇨치료제 ‘글리메피리드’를 섞은 복합제 개발에 나섰다. LG생명과학은 바이오시밀러, 고혈압 복합제 등 다양한 신약과 개량신약 개발을 위한 임상시험에 착수했다. 이 회사의 매출 대비 연구개발비 비율은 20%대로 국내업체 중 가장 높다.
한미약품과 유한양행이 각각 12건, 9건의 임상시험 계획을 승인받으면서 가장 눈에 띄는 신약개발 활동을 펼쳤다.
이밖에 동아제약, 일동제약, 일양약품 등도 신약개발을 위한 적극적인 움직임을 보였다.
▶ 관련기사 ◀
☞[특징주]LG생명과학, 15일째 상승랠리
☞[성공투자 90분] 주가ㆍ업황ㆍ실적 엇박자, 시장 대응 전략은?








![[포토]은행권 소상공인 금융지원 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300609t.jpg)
![[포토]인사청문회 출석한 마은혁 헌법재판관 후보자](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300404t.jpg)
![[포토]아침 영하 10도, 꽁꽁 얼어붙은 도심](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300843t.jpg)
![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)

![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)



