평가 과정에서 상당수 제품이 효과가 없는 것으로 드러나 식약청의 허가 체계에 대한 신뢰성에 물음표를 던지는 시각도 있다. 임상평가의 실효성에 대한 문제점도 노출됐다.
14일 업계에 따르면, 식품의약품안전청은 자하거가수분해물 인태반주사에 대한 임상재평가를 마지막으로 시판중인 인태반 의약품에 대한 평가를 모두 마무리했다.
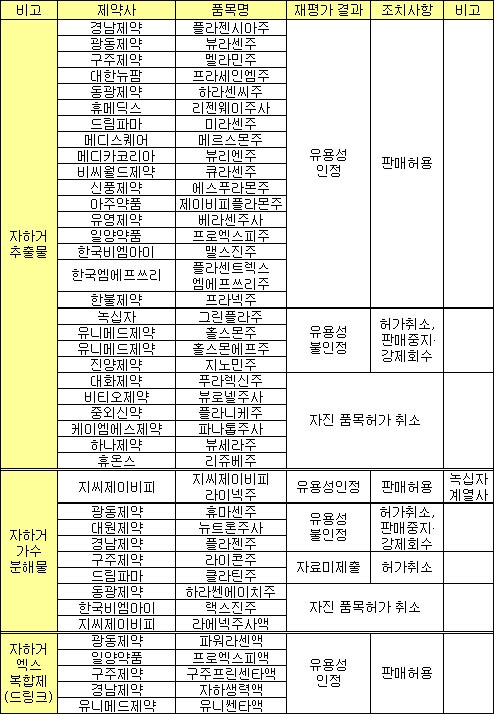
식약청은 인태반의약품의 효능에 대한 의혹이 제기되자 지난 2006년 허가된 제품의 효능을 전면 재검증하는 임상재평가에 착수했다. 재평가는 제품의 특성에 따라 자하거 추출물, 자하거 가수분해물, 자하거엑스 복합제, 등 3분류로 나눠서 진행됐다. ◇시판 제품중 56% 생존..업체별 희비 엇갈리기도
5년에 걸친 평가 결과 자하거 추출물은 27개 품목중 17개, 자하거가수분해물은 9개 품목중 1개, 자하거엑스 복합제는 평가대상 5개 품목 모두 식약청으로부터 효능을 인정받았다. 식약청이 이들 제품의 임상시험 자료를 검토한 결과 판매해도 좋다며 `합격` 판정을 내린 것이다.
식약청으로부터 허가받은 인태반 의약품 41개 품목중 56.1%인 23개 품목만이 생존한 셈이다.
업체별로도 희비가 엇갈렸다. 녹십자(006280)는 연 매출 80억원대를 기록중이던 `그린플라주`가 시장에서 퇴출됐지만 연 매출 200억원대의 `라이넥주`는 임상평가를 통과하며 체면치레를 했다.
광동제약(009290)은 `뷰라센주`와 `파워라센액`가 합격 통지서를 받았지만 `휴마센주`는 시장에서 퇴출됐다. 유니메드제약은 1개 품목이 생존했지만 2개 품목은 시장에서 사라졌다. 일양약품(007570)은 2개 제품 모두 생존하는데 성공했다. ◇임상평가 신뢰성·실효성 물음표 제기 5년여에 걸친 임상평가 과정에서 잡음도 많았다.
태반의약품의 임상평가에 대한 실효성에 물음표를 제기하는 시각도 있었다.
5개 품목 모두 합격한 자하거엑스복합제는 일반의약품으로 분류된 드링크 제품이다. 업계에서는 용법·용량이 명확하지 않은 일반의약품을 임상평가로 효능을 검증하는 것을 두고 식약청의 무리한 행정 남용이라는 불만도 쏟아졌다. 실제로 이들 제품의 검증과정에서도 식약청이 수 차례 전문가 회의를 진행하며 결과 발표가 지연되기도 했다. 식약청 관계자는 "장기간의 임상재평가 결과 23개 제품이 효과가 있는 것으로 결론났다"면서 "향후에는 사후관리를 통해 시판 제품의 안전성 등을 검증할 계획이다"고 말했다.
|
▶ 관련기사 ◀ ☞녹십자, 해외가 성장동력..`매수` -신한 ☞녹십자, `허셉틴` 바이오베터 다국가 임상 개시







![[포토]최상목 경제부총리, '어두운 표정'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400960t.jpg)
![[포토]청사들어서는 한덕수 총리](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400786t.jpg)
![[포토] 대통령실 입구의 취재진](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400817t.jpg)
![[포토]'긴급 의원총회 참석하는 추경호 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400571t.jpg)
![[포토]'긴박했던 흔적들'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400485t.jpg)
![[포토]조국, '국가 비상사태 만든 이는 尹...탄핵해야'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400366t.jpg)
![[포토]尹, '비상 계엄 해제할 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120400277t.jpg)
![[포토]코스피-코스닥 동반 상승 마감](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300908t.jpg)
![[포토]따스한 온기를 퍼지는 행복촌](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300829t.jpg)
![[포토]이웃을 위한 연탄나눔봉사활동](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24120300804t.jpg)



![[속보]민주당 “윤대통령·김용현·이상민, 내란죄 오늘 탄핵 추진”](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24120401019h.jpg)
