7일 식품의약품안전처는 지난해 생동성시험 계획 승인 건수는 163건으로 2012년 201건에 비해 19% 감소했다고 밝혔다. 2010년(388건) 이후 3년 연속 감소세다. 여러 회사가 공동으로 생동성시험을 진행함에 따라 승인 건수가 감소한 것으로 식약처는 분석했다.
당초 식약처은 같은 공장에서 생산되는 똑같은 제네릭이라도 2개사까지만 생동성시험을 진행하도록 제한했지만 불필요한 규제라는 지적에 2011년 말 폐지했다.
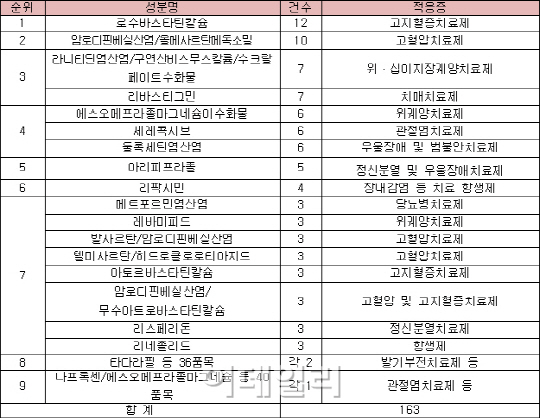
지난해 승인된 생동성시험은 시장성이 높거나 특허만료가 임박한 제품에 집중됐다. 로슈의 고지혈증약 ‘크레스토’와 같은 ‘로수바스타틴칼슘’ 성분 제품을 개발하려는 생동성시험이 12건 진행됐다. 올해 4월 특허 만료 예정인 크레스토는 연간 800억원대의 시장을 형성하고 있다.
치료영역별 승인건수는 심혈관계의약품과 정신신경계의약품이 각각 50건으로 가장 많았다.
식약처 관계자는 “고혈압, 치매 등 고령화 사회에서 발병률이 증가하는 만성질환 치료제와 스트레스 증가 등에 따른 우울장애치료제 및 위ㆍ십이지장궤양치료제 개발에 집중이 계속될 것으로 보인다”고 내다봤다.
|
▶ 관련기사 ◀
☞[특징주]대웅제약, 4Q 부진한 실적에 '약세'
☞대웅제약, 4분기 영업익 기대치 하회..목표가↓-한국
☞대웅제약, 4분기 실적 부진..목표가↓-신한







![[포토]은행권 소상공인 금융지원 간담회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300609t.jpg)
![[포토]인사청문회 출석한 마은혁 헌법재판관 후보자](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300404t.jpg)
![[포토]아침 영하 10도, 꽁꽁 얼어붙은 도심](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122300843t.jpg)
![[포토]스케이트 타는 시민들로 북적](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200317t.jpg)
![[포토]기름값 10주째 올라…전국 휘발유 평균 1652.2원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200258t.jpg)
![[포토]크리스마스 분위기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122200248t.jpg)
![[포토]'서울광장 스케이트장 좋아요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000768t.jpg)
![[포토] 나인퍼레이드 캠페인](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000496t.jpg)
![[포토]더불어민주당 최고위원회의 개최](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122000232t.jpg)


![[포토]안소현-김성태 본부장,취약계증 후원금 전달식 진행](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121400036h.jpg)


