美 FDA, 상반기내 ‘램시마’ 시판 승인 가능성
19일 업계에 따르면 미국 식품의약품국(FDA)은 오는 2월 9일 관절염 관련 자문위원회를 열어 램시마의 허가 여부를 논의할 예정이다. FDA는 자문위원회에서 도출된 의견을 참고해 램시마의 판매 허가에 대한 최종 결정을 내릴 것으로 전망된다.
셀트리온이 지난 2014년 8월 램시마의 FDA 허가를 신청한지 1년 6개월만에 미국 시장 진입이 가시권에 접어든 것이다.
|
램시마가 미국에서 허가받으면 셀트리온(068270)은 해외 진출의 ‘마지막 퍼즐’을 완성하게 되는 셈이다. 램시마는 현재 유럽, 일본, 남미 등 70개국에서 판매를 시작했지만 선진 의약품 시장 중 시장 규모가 가장 큰 미국 시장 진출만 남기고 있었다. 레미케이드는 세계 시장에서 약 10조원어치 팔리는데 이 중 미국 시장의 매출은 절반 가량에 달한다.
미국 판매시 재고 부담↓..실적 논란 해소 전망
셀트리온 바이오시밀러의 해외 유통은 관계사인 셀트리온헬스케어가 담당한다. 셀트리온이 셀트리온헬스케어에 바이오시밀러를 판매하면 셀트리온헬스케어가 해외 유통업체들에 판매하는 방식이다. 셀트리온헬스케어의 매출로 바이오시밀러의 해외 판매 실적을 파악할 수 있다는 의미다. 셀트리온헬스케어의 최대주주는 서정진 셀트리온 회장으로 53.85%의 지분을 보유 중이다.
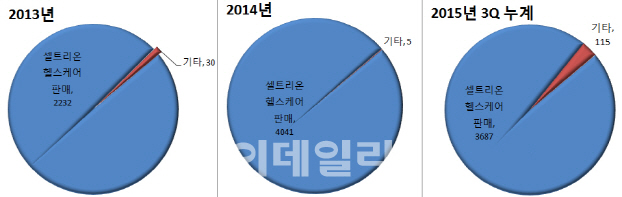
실제로 셀트리온 실적의 대부분은 셀트리온헬스케어 판매매출이 차지한다. 지난해 3분기 누계 셀트리온은 3802억원의 매출을 올렸는데 이중 3687억원은 셀트리온헬스케어에 대한 매출이다. 다국적제약사와의 바이오의약품 생산 대행(CMO) 등으로 올린 매출은 115억원에 불과하다. 셀트리온이 지난해 12월 셀트리온헬스케어와 1192억원 규모의 램시마 공급 계약을 체결, 작년 매출이 5000억원에 육박할 것으로 추정되지만 이 수치로 해외 매출을 판단하기엔 무리가 있다는 의미다.
셀트리온은 지난 2014년에는 매출 4046억원 중 4041억원을 셀트리온헬스케어 판매를 통해 올렸다. 2013년에도 전체 매출에서 셀트리온헬스케어 판매금액이 차지하는 비중은 98.7%에 달했다.
|
|
셀트리온헬스케어가 원료 및 완제품 형태로 보유중인 재고 물량도 사용기한이 충분히 남아있기 때문에 감가상각이 적용되지 않는다는 게 셀트리온 측 설명이다.
셀트리온 “지난해부터 유럽 등 해외 매출 급증”
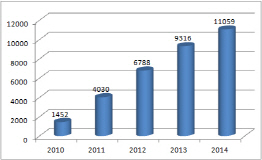
이미 셀트리온 입장에서는 재고부담이 감소하고 있는 것으로 추정된다. 비상장사인 셀트리온헬스케어는 매출을 공개하고 있지 않지만 지난해 상반기에만 전년동기대비 약 250% 성장한 2억6362억달러(약 3180억원)의 수출 실적을 올리며 한국무역협회로부터 ‘3억불 수출의 탑’을 수상하기도 했다.
지난해부터 유럽을 중심으로 램시마의 해외 판매가 본격적으로 늘면서 셀트리온헬스케어의 재고자산도 감소 추세에 접어들 것으로 관측된다. 여기에 미국 판매가 시작되면 ‘셀트리온→셀트리온헬스케어→해외 유통업체’로 이어지는 매출 구조도 안정적인 상승세를 나타낼 것으로 회사 측은 기대하고 있다.
셀트리온 관계자는 “크로아티아, 노르웨이, 벨기에, 네덜란드 등에서는 이미 램시마가 오리지널 레미케이드 시장의 50% 이상을 잠식할 정도로 램시마의 선호도가 높아지는 추세다”면서 “미국 시장에서도 판매가 시작되고 후속 바이오시밀러 제품의 허가가 이뤄지면 실적도 안정적인 상승세를 나타낼 것”으로 기대했다.
▶ 관련기사 ◀
☞ 美 FDA, 내달 셀트리온 '램시마' 허가 여부 논의










![[포토] 평창고랭지 김장축제](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111501303t.jpg)
![[포토] 종로학원, 대입 합격점수 예측 설명회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111501114t.jpg)
![[포토]이재명 민주당 대표 '징역 1년에 집행유예 2년'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111501110t.jpg)
![[포토]'구속VS무죄' 이재명 공판 앞두고 쪼개진 서초동](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111500881t.jpg)
![[포토] 개인정보보호위원회 기자설명회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111500752t.jpg)

![[포토]고생했어~](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111401524t.jpg)
![[포토] 걷고 싶은 거리](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111401206t.jpg)
![[포토] 광복 80주년 기념사업 시민위원회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111401169t.jpg)
![[포토]1400원 뚫은 원-달러 환율…외환당국 '적극개입' 시그널](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111401121t.jpg)

![[이車어때]"8800만원짜리 드림카"…벤츠 AMG A 45 S 4MATIC+](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24111600211h.jpg)
![“일 멈추고 멍 때리세요”…매일 ‘멍시’ 주는 이 회사[복지좋소]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24111600042b.jpg)

![#징역받은#이재명#쾌재부른#여당#침통한#야당#향후#대권은[국회스타그램]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24111600272h.jpg)