|
최근 서울 마곡 본사에서 이데일리와 만난 김종균 프로젠 대표이사는 개발 중인 비만·당뇨치료제 PG-102에 자신감을 보였다. 지난달 식품의약품안전처로부터 임상 2상 승인을 받은 PG-102는 올 연말까지 2상 환자투약을 마치는 것을 목표로 한다.
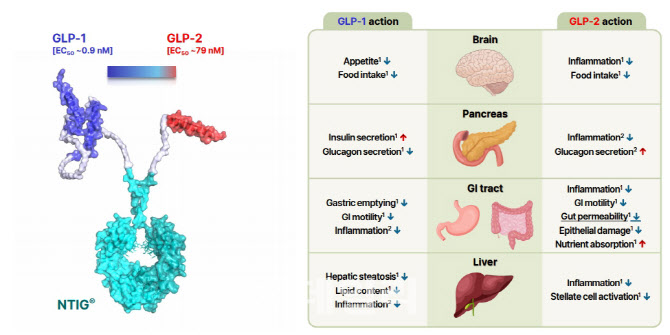
그는 지난 2017년 처음 GLP-2와 GLP-1의 수용체를 동시에 타깃해보자는 아이디어를 갖고 대사이상관련 지방간염(MASH) 치료제로 개발에 돌입했다고 했다. “7년 전은 GLP-1와 관련된 약물들은 이미 개발되던 시기지만 큰 주목을 받지는 못했을 때였다”는 것이 그의 설명이다. 당시 GLP-1 계열 약물은 염증억제기전도 밝혀졌었는데 여기에 GLP-1과 마찬가지로 장 분비 호르몬인 GLP-2를 더하면 장 건강 개선으로 MASH를 개선하고 이와 관련된 대사질환 예방 및 치료에 도움이 될 수 있겠다는 판단에서였다.
그는 “MASH 치료제로 개발하던 중 PG-102의 전신이었던 신약후보물질이 동물실험에서 혈당 및 체중 개선효과가 나타나는 것을 보고 2020년부터는 비만·당뇨치료제로 타깃을 바꿔 집중하기 시작했다”고 설명했다. 이후 GLP-1과 GLP-2의 활성을 조절해 최적화한 것이 지금의 PG-102다.
NTIG는 지난 2005년 프로젠과 제넥신(095700), 포항공대가 공동 개발한 지속형 바이오베터 기술인 하이브리드 Fc 기술(hyFc)을 모태로 한다. 단백질의 안정성 및 혈중 반감기를 높여 1주 제형부터 월 단위 제형까지 확장이 가능하다는 것이 대표적인 특징이다.
|
NTIG의 또 다른 장점은 GLP-1 등 포함한 이중타깃에 선택적으로 결합할 수 있는 하이브리드 펩타이드 방식의 약물과 달리 NTIG 하나에 GLP-1과 GLP-2 펩타이드를 양쪽에 융합시켜 두 타깃에 동시 결합할 수 있다는 점이다. 김 대표는 “대표적으로 일라이 릴리의 ‘마운자로’와 질랜드파마의 다피글루타이드가 하이브리드 펩타이드 형태인데, PG-102가 이들 약물 대비 비임상 동물시험에서 혈당조절 및 체중감소 효과가 우수했던 원인 중 하나가 이중타겟 물질구조이기 때문이었다”고 설명했다. 프로젠은 PG-102이 일반적인 이중항체 단백질보다도 생산성이 2배 이상 높아 상용화시 월 1000~1300달러 수준의 현재 비만치료제보다 가격경쟁력이 클 것으로 봤다.
프로젠은 먹는 비만·당뇨치료제 개발도 전임상연구를 진행 중이다. 지난 6월 말 미국 라니테라퓨틱스와 경구용 비만치료제 RPG-102/RT-114의 공동개발 계약을 체결하면서 관련 연구도 본 궤도에 올랐다. 양사는 내년 1분기 호주 임상 1상 개시를 목표로 협업하고 있다. 김 대표는 “앞서 라니테라퓨틱스가 피하주사(SC) 제형 자가면역질환 치료제 ‘스텔라라’의 바이오시밀러를 자사 플랫폼 기반의 경구약으로 개발했을 때 생체이용률이 84%에 달했다”며 “바이오의약품의 일반적인 경구약 전환 기술은 생체이용률 1%를 넘기 쉽지 않은데 84%라는 숫자를 냈다는 점에서 우리도 기대감이 크다”고 했다. 라니테라퓨틱스는 현재 셀트리온(068270)과 먹는 스텔라라 바이오시밀러 개발을 진행 중이다.
프로젠은 GLP-1과 GLP-2 수용체 이중작용제를 중심으로 다양하게 파이프라인을 확장할 계획이다. 김 대표는 “우선은 PG-102를 비만·당뇨치료제로 먼저 개발하고 비만·당뇨 환자들에게 흔한 합병증인 심장질환, 간 질환, 신장질환을 타깃으로 적응증을 넓혀갈 것”이라며 “GLP-1과 GLP-2 수용체 이중작용제는 기본으로 가져가면서 여기에 다른 인크레틴 유사체를 더하는 후속 파이프라인 개발도 진행 중”이라고 했다. 프로젠은 최근 연관성이 확인되고 있는 알츠하이머, 파킨슨 등의 질환 치료제나, 동물 비만·당뇨치료제로의 개발 가능성도 타진 중이다.
“PG-102의 임상 1상 반복투여용량증량 시험(MAD)를 마친 뒤 임상 1상 데이터를 기반으로 국내 및 아시아 권역을 대상으로 기술이전을 추진할 예정입니다. 임상 2상은 내년 1분기까지 결과를 확보하는 것이 목표인데 이후 글로벌 기술이전을 함께 추진하려고 합니다. 신속한 후기 임상 개발을 통해 오는 2027년 국내 허가 및 조기 상업화가 목표입니다.”










![[포토]잠시 쉬어가는 서울야외도서관](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111000281t.jpg)
![[포토]‘코리아세일페스타’ 개막…숙박·놀이공원·학습지 등 신규 참여](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111000259t.jpg)
![[포토]정부, ‘비위 혐의 다수 발견’ 이기흥 체육회장 등 경찰 수사 의뢰](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111000227t.jpg)
![[포토]수능대박을 위해](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111000202t.jpg)
![[포토]가을의 추억](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24111000165t.jpg)
![[포토]이보미,오랜만에 쉽지않네](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110900387t.jpg)
![[포토] 이대한 '오늘 홀인원 한 볼입니다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110900174t.jpg)
![[포토]박현경,반가운 시선](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110900018t.jpg)
![[포토] 가축분 고체연료 협약 인사말하는 김준동 남부발전 사장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110801640t.jpg)
![[포토] 장유빈 '정교함까지 장착한 장타자'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110800230t.jpg)
![[포토]김재희-홍지원,콤비 즐거운 출발 인사](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24111000266h.jpg)



![노인 타깃의 '이것'....30대 청년이 먹었더니 '오?' [먹어보고서]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/11/PS24111000174h.jpg)