|
에스디바이오센서에 따르면 세계보건기구(WHO)는 코로나19 증상 발현 후 5~7일 이내에 신속항원진단검사를 권고하고 있으므로 FIND는 코로나19 신속항원진단검사를 평가하면서 증상 발현일 기준과 유전자증폭값(PCR Ct)값에 나눠 성능 자료를 도출하고 있다. Ct값은 유전자 증폭 횟수로 Ct값이 낮다는 것은 그만큼 검체에 코로나19 바이러스 유전자가 많아 빨리 확인됐다는 얘기가 된다.
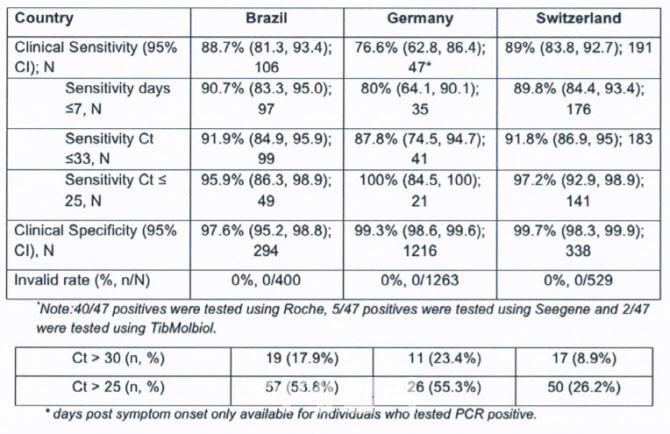
그러면서 “증상 발현일로부터 7일 이내의 검체에 대한 민감도는 88.96%, 특이도는 99.1%이며, Ct값이 33 이하로 낮은 수준의 검체에서 민감도 91.33%, 특이도 99.08%로써 제품의 성 능을 인정받아 전 세계 최초로 WHO로부터 긴급사용승인을 받았다”고 강조했다.
에스디바이오센서는 국제기구의 코로나19 진단시약 구매 연합인 ACT-A를 통해 전 세계에 코로나19 신속항원진단시약을 대량으로 공급하고 있으며 전 세계 약 150여개국에 허가 절차를 완료해 수억 테스트 이상을 수출하고 있다. 미국뿐만 아니라 최근 유럽 국가들에서도 신속항원진단의 유용성을 인정해 사용 확대를 목적으로 자가진단제품 대한 특별허가를 진행하고 있다는 설명이다. 회사의 신속항원진단키트는 독일, 체코,덴마크, 오스트리아, 스위스,네덜란드,포르투갈,슬로바이키아 등 특별허가를 획득한 상태다.
앞서 서울대학교병원 감염내과 김남중 교수 연구팀은 최근 에스디바이오센서의 신속항원검사(Standard Q COVID-19 Ag)와 실시간 유전자 증폭(PCR)검사의 코로나19 진단 능력을 비교한 연구결과를 대한의학회지(JKMS)에 게재했다. 연구팀은 “검사결과 PCR검사와 비교해 신속항원검사의 전반적인 민감도는 17.5%, 특이도는 100%로 확인됐다”고 밝혔다. 이어 “신속항원검사는 높은 특이도에도 불구하고 낮은 민감도로 인해 최적의 임상테스트가 아닐 수 있음을 확인했다”며 “검사를 위한 신속항원진단검사의 가치는 추가 평가가 필요하다”고 지적했다.













![[포토]박현경,책에서 많은 것을 배워요](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121100158t.jpg)
![[포토]윤석열 대통령을 지지 화환](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121101030t.jpg)
![[포토]내란 행위 긴급 현안질문, '질의하는 조국 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121101036t.jpg)
![[포토] 서울시청 방문한 관광객](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121100905t.jpg)
![[포토]한국경제 생산성 제고를 위한 개혁방안](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121100824t.jpg)
![[포토] 서울시 비상경제회의](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121100621t.jpg)
![[포토]법사위 전체회의](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121100594t.jpg)
![[포토]탄핵 정국 연말 특수 기회 사라진 식당](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121001231t.jpg)

![[포토]조정훈-조지연, '비공개 의원총회 참석'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24121000859t.jpg)

![[포토]박현경,자기 관리 중요해요](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24121100160h.jpg)


